题目内容
【题目】高温下焦炭、石英砂的混合物与氯气反应可生成SiCl4。以下是实验室制备SiCl4的装置示意图(注:S1Cl4遇水易水解)。
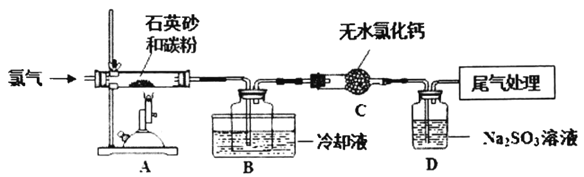
请回答:
(1)用MnO2和浓盐酸制取氯气,为了得到纯净干燥的氯气,可将制得的氯气依次通过盛有____、浓硫酸的洗气瓶。
(2)装置C的作用是______。
(3)设计一个实验方案,用化学方法检验装置D中生成的SO42-_______________。
【答案】 饱和食盐水 避免水蒸气进入B,防止SiCl4水解 取少量D中溶液于试管中,先加入足量稀盐酸,再加入BaCl2,若有白色沉淀产生,说明含有SO42-
【解析】(1)实验室用MnO2和浓盐酸制取氯气,制得的氯气中含有HCl气体和水蒸气,饱和的食盐水可以吸收HCl气体,不会吸收氯气,因此为了得到纯净干燥的氯气,可将制得的氯气先通过饱和的食盐水、再通过浓硫酸。答案为:饱和食盐水
(2)SiCl4遇水易水解,利用装置C吸收水蒸气,避免水蒸气进入B中,防止SiCl4水解。答案为:避免水蒸气进入B,防止SiCl4水解
(3)检验SO42-的方法是先加过量的盐酸,再加BaCl2溶液,因此设计的实验方案为:取少量D中溶液于试管中,先加入足量稀盐酸,再加入BaCl2,若有白色沉淀产生,说明含有SO42-
答案为:取少量D中溶液于试管中,先加入足量稀盐酸,再加入BaCl2,若有白色沉淀产生,说明含有SO42-

练习册系列答案
相关题目