题目内容
【题目】高分子聚合物P的合成路线如图:
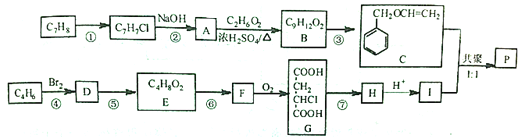
(1)写出反应所需试剂与条件。反应①___;反应⑦___。
(2)写出反应类型:反应③___;反应⑥___。
(3)写出结构简式.E___;P___。
(4)设计反应⑥⑦的目的是___。
(5)写出用1,3-丁二烯与乙酸为原料合成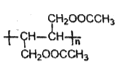 的合成路线(无机原料任选)___。
的合成路线(无机原料任选)___。
(合成路线的常用表示方法为:A![]() B……
B……![]() 目标产物)
目标产物)
【答案】氯气、光照 氢氧化钠的醇溶液、加热 消去反应 加成反应 HOCH2CH=CHCH2OH  或
或 防止碳碳双键被氧化
防止碳碳双键被氧化 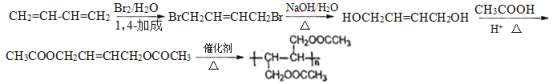
【解析】
结合C的结构简式可知C7H8为![]() ,由转化关系可知,甲苯与氯气在光照条件下发生取代反应生成C7H7Cl为
,由转化关系可知,甲苯与氯气在光照条件下发生取代反应生成C7H7Cl为![]() ,再发生水解反应得到A为
,再发生水解反应得到A为![]() ,苯甲醇与乙二醇褪去1分子式水得到B为
,苯甲醇与乙二醇褪去1分子式水得到B为![]() ,B发生消去反应生成C(
,B发生消去反应生成C(![]() ).根据G的结构简式与转化关系可知,C4H6为CH2=CHCH=CH2,与溴发生1,4-加成生成D为BrCH2CH=CHCH2Br,D发生水解反应得到E为HOCH2CH=CHCH2OH,E发生与HCl发生加成反应得到F为HOCH2CH2CHClCH2OH,F发生氧化反应得到G,G发生消去反应、酸化得到I为HOOCCH=CHCOOH,则H为NaOOCCH=CHCOONa,H和C发生加聚反应生成P,则P的结构简式为:
).根据G的结构简式与转化关系可知,C4H6为CH2=CHCH=CH2,与溴发生1,4-加成生成D为BrCH2CH=CHCH2Br,D发生水解反应得到E为HOCH2CH=CHCH2OH,E发生与HCl发生加成反应得到F为HOCH2CH2CHClCH2OH,F发生氧化反应得到G,G发生消去反应、酸化得到I为HOOCCH=CHCOOH,则H为NaOOCCH=CHCOONa,H和C发生加聚反应生成P,则P的结构简式为: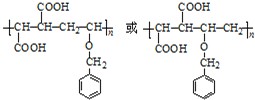 ;
;
(5)要合成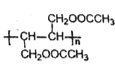 ,可有CH3COOCH2CH=CHCH2OCOCH3发生加聚反应得到,而HOCH2CH=CHCH2OH可与CH3COOH发生酸化反应得到CH3COOCH2CH=CHCH2OCOCH3,而CH2=CH-CH=CH2与Br2发生1,4-加成后,再水解即可制得HOCH2CH=CHCH2OH,由此确定合成流程路线。
,可有CH3COOCH2CH=CHCH2OCOCH3发生加聚反应得到,而HOCH2CH=CHCH2OH可与CH3COOH发生酸化反应得到CH3COOCH2CH=CHCH2OCOCH3,而CH2=CH-CH=CH2与Br2发生1,4-加成后,再水解即可制得HOCH2CH=CHCH2OH,由此确定合成流程路线。
(1)反应①是甲苯与氯气在光照条件下生成![]() ,反应⑦是HOOCCH2CHClCOOH在氢氧化钠醇溶液、加热条件下发生的消去反应;
,反应⑦是HOOCCH2CHClCOOH在氢氧化钠醇溶液、加热条件下发生的消去反应;
(2)反应③为![]() 发生消去反应生成
发生消去反应生成![]() ;反应⑥为HOCH2CH=CHCH2OH与HCl发生加成反应得到HOCH2CH2CHClCH2OH,;
;反应⑥为HOCH2CH=CHCH2OH与HCl发生加成反应得到HOCH2CH2CHClCH2OH,;
(3)E的结构简式为HOCH2CH=CHCH2OH,P的结构简式为: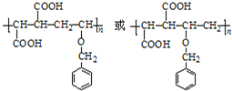 ;
;
(4)反应中⑦中将羟基氧化为羧基,也可以氧化碳碳双键,设计反应⑥⑦的目的是:保护碳碳双键,防止被氧化;
(6)要合成 ,可由CH3COOCH2CH=CHCH2OCOCH3发生加聚反应得到,而HOCH2CH=CHCH2OH与CH3COO发生酸化反应得到CH3COOCH2CH=CHCH2OCOCH3,另外CH2=CH-CH=CH2与Br2发生1,4-加成后,再水解即可制得HOCH2CH=CHCH2OH,则用1,3-丁二烯与乙酸为原料合成
,可由CH3COOCH2CH=CHCH2OCOCH3发生加聚反应得到,而HOCH2CH=CHCH2OH与CH3COO发生酸化反应得到CH3COOCH2CH=CHCH2OCOCH3,另外CH2=CH-CH=CH2与Br2发生1,4-加成后,再水解即可制得HOCH2CH=CHCH2OH,则用1,3-丁二烯与乙酸为原料合成 的合成路线为
的合成路线为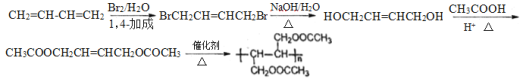 。
。

 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案【题目】超音速飞机在平流层飞行时,尾气中的NO会破坏臭氧层。科学家正在研究利用催化技术将尾气中的NO和CO转变成CO2和N2,其反应为:2NO+2CO![]() 2CO2+N2(降温后该反应的平衡常数变大)为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如表:
2CO2+N2(降温后该反应的平衡常数变大)为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如表:
时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
c(NO)(mol/L) | 1.00×10﹣3 | 4.50×10﹣4 | 2.50×10﹣4 | 1.50×10﹣4 | 1.00×10﹣4 | 1.00×10﹣4 |
c(CO)(mol/L) | 3.60×10﹣3 | 3.05×10﹣3 | 2.85×10﹣3 | 2.75×10﹣3 | 2.70×10﹣3 | 2.70×10﹣3 |
请回答下列问题(均不考虑温度变化对催化剂催化效率的影响):
(1)反应的Q___0(填写“>”、“<”、“=”)。
(2)前2s内的平均反应速率v(N2)=___。
(3)计算在该温度下,反应的平衡常数K=___。
(4)假设在密闭容器中发生上述反应,达到平衡时下列措施能提高NO转化率的是___。
A.选用更有效的催化剂
B.升高反应体系的温度
C.降低反应体系的温度
D.缩小容器的体积
(5)研究表明:在使用等质量催化剂时,增大催化剂比表面积可提高化学反应速率。为了分别验证温度、催化剂比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分实验条件已经填在下面实验设计表中。
实验 编号 | T(℃) | NO初始浓度 (mol/L) | CO初始浓度 (mol/L) | 催化剂的比表面积(m2/g) |
Ⅰ | 280 | 1.20×10-3 | 5.80×10-3 | 82 |
Ⅱ | ___ | ___ | ___ | 124 |
Ⅲ | 350 | ___ | ___ | 124 |
①请在上表空格中填入剩余的实验条件数据。
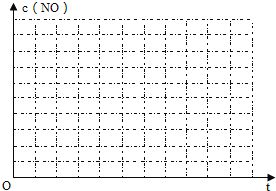
②请在给出的坐标图中,画出上表中的三个实验条件下混合气体中NO浓度随时间变化的趋势曲线图,并标明各条曲线的实验编号___。
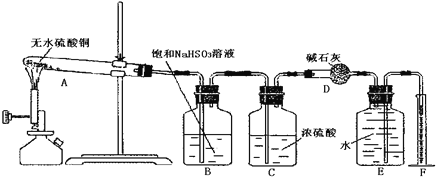
【题目】醋酸亚铬是一种氧气吸收剂, 通常以二水盐[Cr(CH3COO)2]2 ·2H2O(式量:376)的形式存在,难溶于冷水,易溶于盐酸。其制备原理和实验装置:
制备原理:![]()
实验装置:(如图所示)

(1)仪器 A 的名称是__________。
(2)装好试剂后按上述装置进行实验,完成下表内容。
操作步骤 | 实验现象 | 发生反应的离子方程式 |
关闭①___________________,打开②_______________,(用K1、K2、K3填写,下同)使盐酸缓慢加入至抽滤瓶中 | 抽滤瓶中锌粒溶解,溶液由橙色逐渐变成蓝色,有少量气泡 | ③________,Zn+2H+=Zn2++H2↑ |
抽滤瓶中产生大量气体时快速加入适量盐酸,关闭K2和④__________________,打开⑤_________ | 抽滤瓶中⑥____________ | Zn+2H+=Zn2++H2↑ |
当溶液完全转移后,迅速塞紧锥形瓶,用冷水冷却 | 锥形瓶中有深红色晶体析出 | ⑦_____________ |
(3)洗涤产品后干燥、称量,得到 1.0g 固体。列式表示产率:____(不必计算出结果,K2Cr2O7 式量:294)。在实验中如果盐酸过量,会导致产率偏________。(填“高”或“低”)