题目内容
【题目】高铁酸盐是一种高效绿色氧化剂,可用于废水和生活用水的处理。从环境保护的角度看,制备高铁酸盐较好的方法为电解法:Fe+2H2O+2OH![]() FeO42-+3H2↑,工作原理如图所示。己知:Na2FeO4只在强碱性条件下稳定,易被H2还原。下列说法正确的是
FeO42-+3H2↑,工作原理如图所示。己知:Na2FeO4只在强碱性条件下稳定,易被H2还原。下列说法正确的是
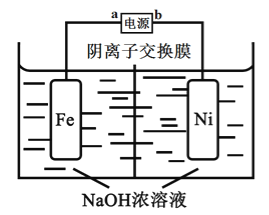
A. b是电源的正极
B. 阳极电极反应为Fe-6e-+4H2O= FeO42-+ 8H+
C. 电解过程中,需要将阴极产生的气体及时排出
D. 当电路中通过1mol电子的电量时,会有11.2L的H2生成
【答案】C
【解析】A、根据方程式可知铁失去电子,铁作阳极,与电源的正极相连,因此a是电源的正极,A错误;B、阳极电极反应为Fe-6e-+8OH-=FeO42-+4H2O,B错误;C、氢气具有还原性,根据题意Na2FeO4只在强碱性条件下稳定,易被H2还原。电解过程中,须将阴极产生的气体及时排出,防止Na2FeO4与H2反应使产率降低,C正确;D、氢气不一定处于标准状况下,不能计算其体积,D错误;答案选C。

练习册系列答案
 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案 名校提分一卷通系列答案
名校提分一卷通系列答案 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案
相关题目
【题目】在25℃时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如下表:
物质 | X | Y | Z |
初始浓度/mol·L-1 | 0.1 | 0.2 | 0 |
平衡浓度/mol·L-1 | 0.05 | 0.05 | 0.1 |
下列说法错误的是:
A. 反应达到平衡时,X的转化率为50% B. 反应可表示为X+3Y![]() 2Z,其平衡常数为1600 C. 增大压强使平衡向生成Z的方向移动,平衡常数增大 D. 改变温度可以改变此反应的平衡常数
2Z,其平衡常数为1600 C. 增大压强使平衡向生成Z的方向移动,平衡常数增大 D. 改变温度可以改变此反应的平衡常数