题目内容
恒温、恒压下,a mol A和b mol B在一个容积可变的容器中发生如下反应:A(g)+2B(g) 2C(g),一段时间后达到平衡,生成n mol C。则下列说法中正确的是( )
2C(g),一段时间后达到平衡,生成n mol C。则下列说法中正确的是( )
A.物质A、B的转化率之比为a∶b
B.当v正(A)=2v逆(B)时,可确定反应到达平衡状态
C.起始时刻和达平衡后容器中的压强比为(a+b)∶(a+b— )
)
D.若起始时放入2a mol A和2b mol B,则达平衡时生成2n mol C
 2C(g),一段时间后达到平衡,生成n mol C。则下列说法中正确的是( )
2C(g),一段时间后达到平衡,生成n mol C。则下列说法中正确的是( )A.物质A、B的转化率之比为a∶b
B.当v正(A)=2v逆(B)时,可确定反应到达平衡状态
C.起始时刻和达平衡后容器中的压强比为(a+b)∶(a+b—
 )
)D.若起始时放入2a mol A和2b mol B,则达平衡时生成2n mol C
D
设转化了x mol A,则转化了2x mol B,转化率之比为: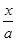 ∶
∶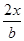 =b∶2a,A项错误;B项应当v正(A)=
=b∶2a,A项错误;B项应当v正(A)=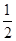 v逆(B)时,确定反应到达平衡状态,错误;题中说明为恒压下反应,C项错误;在恒压下反应,反应物加倍,生成物加倍,D项正确
v逆(B)时,确定反应到达平衡状态,错误;题中说明为恒压下反应,C项错误;在恒压下反应,反应物加倍,生成物加倍,D项正确
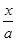 ∶
∶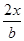 =b∶2a,A项错误;B项应当v正(A)=
=b∶2a,A项错误;B项应当v正(A)=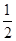 v逆(B)时,确定反应到达平衡状态,错误;题中说明为恒压下反应,C项错误;在恒压下反应,反应物加倍,生成物加倍,D项正确
v逆(B)时,确定反应到达平衡状态,错误;题中说明为恒压下反应,C项错误;在恒压下反应,反应物加倍,生成物加倍,D项正确
练习册系列答案
 优生乐园系列答案
优生乐园系列答案
相关题目
 2C(g)达到平衡状态标志的是( )。
2C(g)达到平衡状态标志的是( )。 2SO3(g) ΔH=-a kJ·mol-1(a>0)。恒温恒容下,在10 L的密闭容器中加入0.1 mol SO2和0.05 mol O2,经过2 min达到平衡状态,反应放热0.025 a kJ。下列判断正确的是( )
2SO3(g) ΔH=-a kJ·mol-1(a>0)。恒温恒容下,在10 L的密闭容器中加入0.1 mol SO2和0.05 mol O2,经过2 min达到平衡状态,反应放热0.025 a kJ。下列判断正确的是( ) 2C(g) ΔH<0。达到平衡后,改变一个条件,下列量(Y)的变化不符合图中曲线的是( )
2C(g) ΔH<0。达到平衡后,改变一个条件,下列量(Y)的变化不符合图中曲线的是( )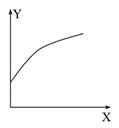
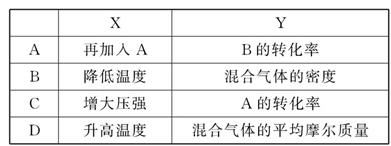
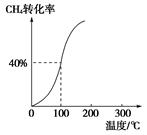
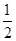 ,其他条件不变,对平衡体系产生的影响是________(填字母序号)。
,其他条件不变,对平衡体系产生的影响是________(填字母序号)。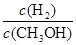 减小
减小 CO(g)+2H2(g),此反应能自发进行的原因是:___。
CO(g)+2H2(g),此反应能自发进行的原因是:___。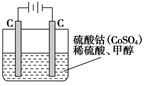
 2CO2(g)+N2(g)可用于净化汽车尾气,已知该反应速率极慢,570 K时平衡常数为1×1059。下列说法正确的是( )
2CO2(g)+N2(g)可用于净化汽车尾气,已知该反应速率极慢,570 K时平衡常数为1×1059。下列说法正确的是( ) N2O4(g) ΔH<0 反应相同时间后,分别测定体系中NO2的百分量(NO2%),并作出其随反应温度(T)变化的关系图。下列示意图中,可能与实验结果相符的是
N2O4(g) ΔH<0 反应相同时间后,分别测定体系中NO2的百分量(NO2%),并作出其随反应温度(T)变化的关系图。下列示意图中,可能与实验结果相符的是