题目内容
【题目】[Zn(CN)4]2-在水溶液中可与HCHO发生反应生成[Zn(H2O)4]2+和HOCH2CN,下列说法错误的是( )
A.Zn2+基态核外电子排布式为[Ar]3d10
B.1mol HCHO分子中含有σ键的数目为1.806×1024
C.HOCH2CN分子中碳原子轨道的杂化类型是sp3
D.[Zn(CN)4]2-中Zn2+与CN-的C原子形成配位键,结构可表示为
【答案】C
【解析】
A.Zn原子序数为30,位于ⅡB族,所以,Zn2+基态核外电子排布式为[Ar]3d10,A选项正确;
B.1分子HCHO含2个C-H键和1个C=O键,共有3个σ键,所以,1molHCHO分子中含有σ键的物质的量为3mol,数目为1.806×1024,B选项正确;
C.HOCH2CN分子中与羟基相连的C为sp3杂化,-CN(-C≡N)中的C为sp杂化,C选项错误;
D.[Zn(CN)4]2-中Zn2+与CN-的C原子形成配位键,Zn为sp3杂化,配位原子形成正四面体,所以,[Zn(CN)4]2-结构可表示为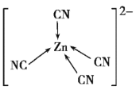 ,D选项正确;
,D选项正确;
答案选C。

练习册系列答案
 快捷英语周周练系列答案
快捷英语周周练系列答案
相关题目