题目内容
【题目】H、C、N、O、Al、S是常见的六种元素.完成下列填空:
(1)碳元素有12C、13C和14C等同位素.在14C原子中,核外存在对自旋相反的电子.
(2)碳在形成化合物时,其所成化学键以共价键为主,原因是 .
(3)任选上述元素可组成多种四原子的共价化合物,请写出其中含非极性键的一种化合物的电子式 .
(4)上述元素可组成盐NH4Al(SO4)2 . 向10mL1mol/L NH4Al(SO4)2溶液中滴加1mol/L的NaOH溶液,沉淀物质的量随NaOH溶液体积的变化示意图如下.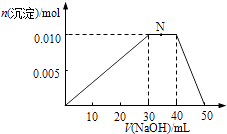
①NH4Al(SO4)2溶液中所有离子的浓度由大到小的顺序是 , 请解释阳离子浓度差异的原因 .
②写出N点反应的离子方程式 .
③若向10mL1mol/L NH4Al(SO4)2溶液中加入20mL1.2mol/LBa(OH)2溶液,充分反应后,产生沉淀mol.
【答案】
(1)2
(2)C有4个价电子且半径较小,难以通过得或失电子达到稳定结构
(3)![]() 或H:CC:H
或H:CC:H
(4)c(SO42﹣)>c(NH4+)>c(Al3+)>c(H+)>c(OH﹣);由于碱性:氨水>Al(OH)3 , 故Al3+的水解程度大于NH4+的水解程度,c(NH4+)>c(Al3+);NH4++OH﹣=NH3H2O;0.022
【解析】解:(1)C原子核外电子排布为1s22s22p2 , 轨道式为如图所示: ![]() ,则在基态14C原子中,核外存在2对自旋相反的电子,故答案为:2;(2)共价键为原子之间以共用电子对成键,碳原子核外有4个电子,且元素的非金属性较弱,但半径较小,反应中难以失去或得到电子,故答案为:C有4个价电子且半径较小,难以通过得或失电子达到稳定结构;(3)上述元素可组成多种四原子的共价化合物,其中含非极性键的物质是H2O2和C2H2 , 电子式分别为
,则在基态14C原子中,核外存在2对自旋相反的电子,故答案为:2;(2)共价键为原子之间以共用电子对成键,碳原子核外有4个电子,且元素的非金属性较弱,但半径较小,反应中难以失去或得到电子,故答案为:C有4个价电子且半径较小,难以通过得或失电子达到稳定结构;(3)上述元素可组成多种四原子的共价化合物,其中含非极性键的物质是H2O2和C2H2 , 电子式分别为 ![]() 、H:CC:H,故答案为:
、H:CC:H,故答案为: ![]() 或H:CC:H;(4)①NH4Al(SO4)2 , 溶液中Al3+、NH4+均水解使溶液呈酸性,由于碱性:氨水>Al(OH)3 , 所以Al3+比 NH4+水解程度更大,c(NH4+)>c(Al3+),故离子浓度由大到小的顺序是:c(SO42﹣)>c(NH4+)>c(Al3+)>c(H+)>c(OH﹣),故答案为:c(SO42﹣)>c(NH4+)>c(Al3+)>c(H+)>c(OH﹣);由于碱性:氨水>Al(OH)3 , 故Al3+的水解程度大于NH4+的水解程度,c(NH4+)>c(Al3+); ②N点过程中加入氢氧化钠,沉淀物质的量不变,是NH4+与OH﹣反应生成NH3H2O,离子方程式为:NH4++OH﹣=NH3H2O,故答案为:NH4++OH﹣=NH3H2O;③10mL 1molL﹣1 NH4Al(SO4)2溶液中Al3+ 物质的量为0.01mol,NH4+的物质的量为0.01mol,SO42﹣的物质的量为0.02mol,20mL 1.2 molL﹣1Ba(OH)2溶液中Ba2+物质的量为0.024mol,OH﹣为0.048mol,由SO42﹣+Ba2+=BaSO4↓,可知SO42﹣不足,故可以得到0.02mol BaSO4 ,
或H:CC:H;(4)①NH4Al(SO4)2 , 溶液中Al3+、NH4+均水解使溶液呈酸性,由于碱性:氨水>Al(OH)3 , 所以Al3+比 NH4+水解程度更大,c(NH4+)>c(Al3+),故离子浓度由大到小的顺序是:c(SO42﹣)>c(NH4+)>c(Al3+)>c(H+)>c(OH﹣),故答案为:c(SO42﹣)>c(NH4+)>c(Al3+)>c(H+)>c(OH﹣);由于碱性:氨水>Al(OH)3 , 故Al3+的水解程度大于NH4+的水解程度,c(NH4+)>c(Al3+); ②N点过程中加入氢氧化钠,沉淀物质的量不变,是NH4+与OH﹣反应生成NH3H2O,离子方程式为:NH4++OH﹣=NH3H2O,故答案为:NH4++OH﹣=NH3H2O;③10mL 1molL﹣1 NH4Al(SO4)2溶液中Al3+ 物质的量为0.01mol,NH4+的物质的量为0.01mol,SO42﹣的物质的量为0.02mol,20mL 1.2 molL﹣1Ba(OH)2溶液中Ba2+物质的量为0.024mol,OH﹣为0.048mol,由SO42﹣+Ba2+=BaSO4↓,可知SO42﹣不足,故可以得到0.02mol BaSO4 ,
Al3++3OH﹣=Al(OH)3↓
0.01mol 0.03mol 0.01mol
反应剩余OH﹣为0.048mol﹣0.03mol=0.018mol,
NH4++OH﹣=NH3H2O
0.01mol 0.01mol
反应剩余OH﹣为0.018mol﹣0.01mol=0.008mol,
Al(OH)3+OH﹣=AlO2﹣+2H2O
0.008mol 0.008mol
故得到Al(OH)3沉淀为0.01mol﹣0.008mol=0.002mol
则最终得到固体为0.02mol+0.002mol=0.022mol,故答案为:0.022.
(1)根据同一轨道的2两个电子自选方向相反判断;(2)共价键为原子之间以共用电子对成键,碳的非金属性较弱,但半径较小,反应中难以失去或得到电子;(3)同种元素的原子之间形成非极性键;(4)①溶液中Al3+、NH4+均水解使溶液呈酸性,但Al3+比 NH4+水解程度更大;②N点过程中加入氢氧化钠,沉淀物质的量不变,是NH4+与OH﹣反应生成NH3H2O;③根据n=cV计算n(Al3+ )、n(NH4+)、n(SO42﹣)、n(Ba2+)、n(OH﹣),根据SO42﹣、Ba2+中不足量的离子的物质的量计算生成BaSO4的物质的量,依次发生:Al3++3OH﹣=Al(OH)3↓、NH4++OH﹣=NH3H2O、Al(OH)3+OH﹣=AlO2﹣+2H2O,根据方程式计算生成Al(OH)3的物质的量,进而二者计算生成固体总物质的量.

 经典密卷系列答案
经典密卷系列答案 金牌课堂练系列答案
金牌课堂练系列答案 三新快车金牌周周练系列答案
三新快车金牌周周练系列答案