题目内容
18.下列式子中不正确的是( )| A. |  | B. |  | ||
| C. |  | D. |  |
分析 化合价升高时元素失去电子,化合价降低时元素得到电子,氧化还原反应中得失电子守恒,据此分析.
解答 解:A、H元素的化合价升高,Cu元素的化合价降低,则H失去电子被氧化,Cu得到电子被还原,转移的电子数为2e-,故A正确;
B、该反应中Cl元素的化合价既升高又降低,转移的电子数为e-,故B正确;
C、该反应中Zn失去电子被氧化,氢得到电子被还原,转移的电子数为2e-,故C正确;
D、该反应中O失去电子被氧化,Cl得到电子被还原,转移的电子数为12e-,故D错误;
故选D.
点评 本题考查氧化还原反应中电子的转移,明确化合价升高的元素失去电子及电子守恒是解答本题的关键,难度不大.

练习册系列答案
 导学与测试系列答案
导学与测试系列答案 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案
相关题目
8.下列变化过程,属于放热反应的是( )
①水蒸气变成液态水
②酸碱中和反应
③浓硫酸稀释
④固体氢氧化钠溶于水
⑤氢气在氯气中燃烧
⑥食物腐败.
①水蒸气变成液态水
②酸碱中和反应
③浓硫酸稀释
④固体氢氧化钠溶于水
⑤氢气在氯气中燃烧
⑥食物腐败.
| A. | ②③④⑤⑥ | B. | ②③④ | C. | ②⑤⑥ | D. | ①③⑤ |
9.水的三态的熵值的大小关系正确的是( )
| A. | S (s)>S (l)>S (g) | B. | S (g)>S (l)>S (s) | C. | S (l)>S (s)>S (g) | D. | S (g)>S (s)>S (l) |
6.在四个不同的容器中,在不同的条件下进行合成氨反应N2+3H2?2NH3,根据下列在相同时间内测得的结果判断,生成氨的反应速率最快的是( )
| A. | v(NH3)=0.3 mol/(L•min) | B. | v(N2)=0.01 mol/(L•s) | ||
| C. | v(N2)=0.2 mol/(L•min) | D. | v(H2)=0.3 mol/(L•min) |
13.下列各组中的物质属于同一类别(指酸、碱、盐、氧化物)的是( )
| A. | 烧碱、纯碱、熟石灰 | B. | 纯碱、胆矾、硫酸钠 | ||
| C. | 干冰、冰、金刚石 | D. | 氯化钙、氧化钙、硝酸钙 |
3.只用一种试剂,可以一次性鉴别NH4Cl、NaCl、Na2SO4三种溶液,这种试剂是( )
| A. | Ba(OH)2溶液 | B. | KCl溶液 | C. | 酚酞溶液 | D. | 盐酸 |
10.在用Zn、Cu片和稀H2SO4组成的原电池装置中,经过一段时间工作后,下列说法中正确的是( )
| A. | 锌片是正极,铜片上有气泡产生 | B. | 溶液中H2SO4 的物质的量减少 | ||
| C. | 电流方向是从锌片流向铜片 | D. | 电解液的pH保持不变 |
7.焙制糕点时,常用到小苏打粉,小苏打的化学式为( )
| A. | NaNO3 | B. | Na2CO3 | C. | NaHCO3 | D. | Na2SO4 |
8. 25℃时,部分物质的电离常数如表所示:
25℃时,部分物质的电离常数如表所示:
请回答下列问题:
(1)a.CH3COOH,b.H2CO3,c.HClO的酸性由强到弱的顺序为a>b>c(填编号).
(2)同浓度的a.CH3COO-,b.HCO${\;}_{3}^{-}$,c.CO${\;}_{3}^{2-}$,d.ClO-结合H+的能力由强到弱的顺序为c>d>b>a(填编号).
(3)向NaClO溶液中通入少量的CO2,反应的离子方程式为ClO-+CO2+H2O=HCO3-+HClO.
(4)pH相同的下列四种物质的溶液:a.Na2CO3,b.NaClO,c.CH3COONa,d.NaHCO3,物质的量浓度由大到小的顺序是c>d>b>a(填编号).
(5)常温下0.1mol•L-1的CH3COOH溶液在加水稀释过程中,下列表达式的数据一定变小的是A(填序号).
A.c(H+) B.c(H+)/c(CH3COOH)
C.c(H+)•c(OH-) D. c(H+)•c(CH3COO-)/c(CH3COOH)
若该溶液升高温度,上述5种表达式的数据增大的是ABCD.
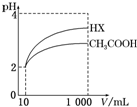
(6)体积为10mL pH=2的醋酸溶液与一元酸HX分别加水稀释至1 000mL,稀释过程中pH变化如图所示,则HX的电离常数大于(填“大于”、“等于”或“小于”)醋酸的电离常数;稀释后,HX溶液中由水电离出来的c(H+)大于(填“大于”、“等于”或“小于”)醋酸溶液中由水电离出来的c(H+).
 25℃时,部分物质的电离常数如表所示:
25℃时,部分物质的电离常数如表所示:| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离常数 | 1.7×10-5 | K1=4.3×10-7 K2=5.6×10-11 | 3.0×10-8 |
(1)a.CH3COOH,b.H2CO3,c.HClO的酸性由强到弱的顺序为a>b>c(填编号).
(2)同浓度的a.CH3COO-,b.HCO${\;}_{3}^{-}$,c.CO${\;}_{3}^{2-}$,d.ClO-结合H+的能力由强到弱的顺序为c>d>b>a(填编号).
(3)向NaClO溶液中通入少量的CO2,反应的离子方程式为ClO-+CO2+H2O=HCO3-+HClO.
(4)pH相同的下列四种物质的溶液:a.Na2CO3,b.NaClO,c.CH3COONa,d.NaHCO3,物质的量浓度由大到小的顺序是c>d>b>a(填编号).
(5)常温下0.1mol•L-1的CH3COOH溶液在加水稀释过程中,下列表达式的数据一定变小的是A(填序号).
A.c(H+) B.c(H+)/c(CH3COOH)
C.c(H+)•c(OH-) D. c(H+)•c(CH3COO-)/c(CH3COOH)
若该溶液升高温度,上述5种表达式的数据增大的是ABCD.
(6)体积为10mL pH=2的醋酸溶液与一元酸HX分别加水稀释至1 000mL,稀释过程中pH变化如图所示,则HX的电离常数大于(填“大于”、“等于”或“小于”)醋酸的电离常数;稀释后,HX溶液中由水电离出来的c(H+)大于(填“大于”、“等于”或“小于”)醋酸溶液中由水电离出来的c(H+).