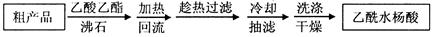题目内容
硫代硫酸钠(Na2S2O3)俗称保险粉,可用作定影剂,也可用于纸浆漂白、脱氯剂等。
Na2S2O3易溶于水,不溶于乙醇,常温下溶液中析出晶体通常为Na2S2O·5H2O。实验室制备保险粉的装置如下图所示。涉及的总化学方程式如下: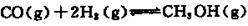
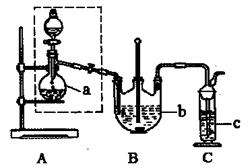
(1)检查虚线框内装置气密性的方法是 。
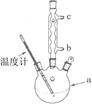
(2)反应前仪器a中加入的药品为 ,仪器c中加入的药品为 。
(3)仪器b的名称是 。
(4)在制备过程中,持续通人气体时,观察到B装置中先有大量浅黄色沉淀析出,反应一段时间,沉淀逐渐减少;待浅黄色沉淀消失时反应完成,停止加热。反应的离子方程式为 。
(5)反应完成后,为了从混合溶液中获取产品,操作如下:
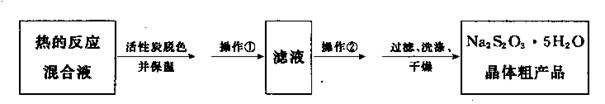
操作②为 。
(6)为了测产品的纯度,称取8.000 g粗产品,配制成250 mL溶液,用移液管移取25.00 mL于锥形瓶中,再用0.05000 mol·L-l的碘标准溶液进行滴定(2S2O32-+I2=S4O62-+2I-),
平行3次实验,平均消耗碘标准溶液的体积为30.00mL。
①测得产品的纯度为 。
②关于上述实验的有关操作,以下表述正确的是 。(填编号)
Na2S2O3易溶于水,不溶于乙醇,常温下溶液中析出晶体通常为Na2S2O·5H2O。实验室制备保险粉的装置如下图所示。涉及的总化学方程式如下:
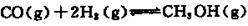

(1)检查虚线框内装置气密性的方法是 。
(2)反应前仪器a中加入的药品为 ,仪器c中加入的药品为 。
(3)仪器b的名称是 。
(4)在制备过程中,持续通人气体时,观察到B装置中先有大量浅黄色沉淀析出,反应一段时间,沉淀逐渐减少;待浅黄色沉淀消失时反应完成,停止加热。反应的离子方程式为 。
(5)反应完成后,为了从混合溶液中获取产品,操作如下:

操作②为 。
(6)为了测产品的纯度,称取8.000 g粗产品,配制成250 mL溶液,用移液管移取25.00 mL于锥形瓶中,再用0.05000 mol·L-l的碘标准溶液进行滴定(2S2O32-+I2=S4O62-+2I-),
平行3次实验,平均消耗碘标准溶液的体积为30.00mL。
①测得产品的纯度为 。
②关于上述实验的有关操作,以下表述正确的是 。(填编号)
| A.用碱式滴定管盛装碘标准溶液 |
| B.用移液管移取25.00mL溶液于锥形瓶中,移液管的尖嘴和锥形瓶内壁要接触 |
| C.如果滴定终点没有控制好,碘标准溶液滴加过量,则必须重新进行滴定 |
| D.滴定过程中若剧烈摇动锥形瓶(溶液不外溅),则所测得的纯度将会偏高 |
(1)关闭蒸馏烧瓶右端活塞,往分液漏斗中加水,打开分液漏斗的活塞,水开始下滴,一段时间后,如果水不再下滴,表明气密性良好。反之则气密性不好。
(2)Na2SO3固体 NaOH溶液(或KMnO4溶液等)
(3)三颈烧瓶
(4)S2O32-+SO2+H2O=S↓+2HSO32-
(5)蒸发浓缩、冷却结晶
(6)①93.00% ②B
(2)Na2SO3固体 NaOH溶液(或KMnO4溶液等)
(3)三颈烧瓶
(4)S2O32-+SO2+H2O=S↓+2HSO32-
(5)蒸发浓缩、冷却结晶
(6)①93.00% ②B
试题分析:(1)检查虚线框内装置气密性的方法是关闭蒸馏烧瓶右端活塞,往分液漏斗中加水,打开分液漏斗的活塞,水开始下滴,一段时间后,如果水不再下滴,表明气密性良好。反之则气密性不好。(2)装置A是制取SO2的,反应前仪器a中加入的药品为Na2SO3固体,在分液漏斗内加入稀盐酸或稀硫酸。分数反应为:Na2SO3+H2SO4= Na2SO4+SO2↑+H2O;在装置B中加入Na2S。发生反应2Na2S+3SO2=2Na2SO3+3S ;Na2SO3+S=Na2S2O3。由于SO2或H2S都是大气污染物,所以未完全转化为Na2S2O3的SO2或H2S在装置C中被吸收。SO2或H2S都是酸性气体,同时也有还原性,所以仪器c中加入的药品为NaOH溶液(或KMnO4溶液等) 。(3)仪器b的名称是三颈烧瓶。(4)根据题意可得该反应的离子方程式为S2O32-+SO2+H2O=S↓+2HSO32-。(5)操作②从溶液中结晶析出晶体的操作是蒸发浓缩、冷却结晶。(6) ①由方程式2S2O32-+I2=S4O62-+2I-。可得n(Na2S2O3)=2n(I2)= 2×(0.05000 mol/L×0.03L)×(250 mL÷25.00 mL)=0.03mol.所以测得产品的纯度为(0.03mol×248g/mol)÷8.000g×100%="93.00%." ②A.碘单质有强的氧化性,容易腐蚀橡胶管,所以用酸式滴定管盛装碘标准溶液。错误。B.用移液管移取25.00mL溶液于锥形瓶中时,悬于移液管的尖嘴的液体是在量取体积范围内的,所以要和锥形瓶内壁要接触,使其滴入锥形瓶中。正确。C.测定样品的纯度就是以碘标准溶液为标准的,如果滴定终点没有控制好,碘标准溶液滴加过量,则可通过反滴加待测溶液。根据反应时二者的体积关系进行纯度的计算没有必须重新进行滴定。错误。D.滴定过程中若剧烈摇动锥形瓶,只要溶液不外溅,则二者就可以充分进行反应。所以对所测得的纯度无影响。错误。选项为B。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
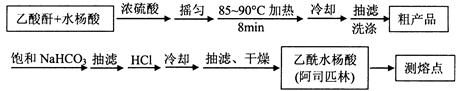
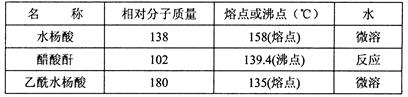
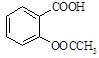 )是世界上应用最广泛的解热、镇痛和抗炎药。乙酰水杨酸受热易分解,分解温度为128~135℃。某学习小组在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成阿司匹林,制备基本操作流程如下:
)是世界上应用最广泛的解热、镇痛和抗炎药。乙酰水杨酸受热易分解,分解温度为128~135℃。某学习小组在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成阿司匹林,制备基本操作流程如下: