题目内容
盖斯定律指出:化学反应的焓变只与各反应物的始态和各生成物的终态有关,而与具体的反应途径无关。物质A在一定条件下可发生一系列转化,由图判断下列关系错误的是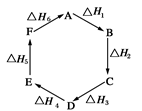
| A.A→F,ΔH=-ΔH6 |
| B.ΔH1+ΔH2+ΔH3+ΔH4+ΔH5+ΔH6=1 |
| C.C→F,|ΔH|=|ΔH1+ΔH2+ΔH6| |
| D.|ΔH1+ΔH2+ΔH3|=|ΔH4+ΔH5+ΔH6| |
B
解析试题分析:从反应图像来看,ΔH1+ΔH2+ΔH3+ΔH4+ΔH5+ΔH6表示从A又回到A,整个过程中没有能量变化,所以ΔH1+ΔH2+ΔH3+ΔH4+ΔH5+ΔH6=0,B项错误,答案选B。
考点:盖斯定律
点评:化学反应中的能量变化只与反应物和产物的状态有关,与反应的路径无关。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
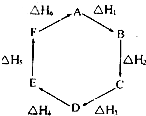 盖斯定律指出:化学反应的反应热只与反应的始态(各反应物)和终态(各生成物)有关,而与具体反应进行的途径无关.物质A在一定条件下可发生一系列转化,如图判断下列关系正确的是( )
盖斯定律指出:化学反应的反应热只与反应的始态(各反应物)和终态(各生成物)有关,而与具体反应进行的途径无关.物质A在一定条件下可发生一系列转化,如图判断下列关系正确的是( )| A、A→F,△H=-△H 6 | B、△H1+△H 2+△H 3+△H 4+△H 5+△H 6=1 | C、C→F,△H=△H 1+△H 2+△H 6 | D、△H 1+△H 2+△H 3═△H 4+△H5+△H 6 |
盖斯定律指出:化学反应的反应热只与反应的始态(各反应物)和终态(各生成物)有关,而与具体反应进行的途径无关.物质A在一定条件下可发生一系列转化,由图判断下列关系错误的是( )
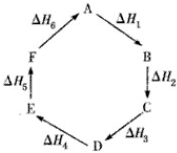

| A、C→F,|△H|=|△H1+△H2+△H6| | B、△H1+△H2+△H3+△H4+△H5+△H6=0 | C、A→F,△H=△H6 | D、|△H1+△H2+△H3|=|△H4+△H5+△H6| |
 盖斯定律指出:化学反应的焓变只与各反应物的始态和各生成物的终态有关,而与具体的反应途径无关.物质A在一定条件下可发生一系列转化,由图判断下列关系错误的是( )
盖斯定律指出:化学反应的焓变只与各反应物的始态和各生成物的终态有关,而与具体的反应途径无关.物质A在一定条件下可发生一系列转化,由图判断下列关系错误的是( )