题目内容
本题包括A、B两小题,分别对应于“物质结构与性质”和“实验化学”两个选修模块的内容。请选定其中一题,并在相应的答题区域内作答。若两题都做,则按A题评分。
A.诺贝尔物理学奖曾授予Henry Bragg和Lawrence Bragg,以表彰他们用X射线对晶体结构的分析所作的贡献。
(1)在硼酸[B(OH)3]分子中,B原子与3个羟基相连,其晶体具有与石墨相似的层状结构。则分子中B原子杂化轨道的类型为 ,同层分子间的主要作用为 。
 (2)K3[Fe(CN)6]晶体中含有的化学键类型为 ,
(2)K3[Fe(CN)6]晶体中含有的化学键类型为 ,
Fe3+与CN-之间能够形成化学键的原因是 。
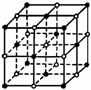
(3)等物质的量的氧化物MO与SiC的电子总数相等,则M2+
离子的核外电子排布式为 。
MO是优良的耐高温材料,其晶体结构与NaCl晶体相
似,晶体中与每个M2+等距离且最近的几个O2-所围成
的空间几何构型为 。
MO的熔点比CaO的高,原因是 。
B.某化工废液中可能含有下列微粒:Al3+、Fe3+、NO2-、甘油分子。化学兴趣小组的同学设计了下列实验验证这些微粒的存在。
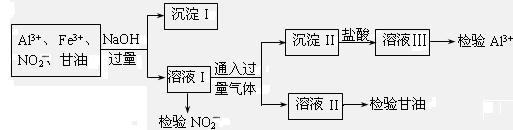
(1)分离出沉淀I的操作名称是 ,利用沉淀I可检验出 离子。
(2)通入的过量气体是 。(写化学式)
(3)用酸性KI溶液检验NO2-离子的离子方程式为 。
(4)写出检验甘油所发生反应的化学方程式: 。
(5)若向溶液III中先加足量NH4F后加氨水来检验Al3+离子,则能否达到目的?
答: (填“能”或“不能”);原因是 。
共12分。
A.(1)sp2(1分) 氢键(1分) (2)离子键、极性共价键、配位键(2分)
CN-能提供孤对电子,Fe3+能接受孤对电子或Fe3+有空轨道(2分)
(3)1s22s22p6(2分) 正八面体(2分)
Mg2+半径比Ca2+的小,MgO的晶格能大(2分)
B.(1)过滤(1分) Fe3+(1分) (2)CO2(2分)
(3)2NO2- + 2I- + 4H+=2NO↑ + I2 + 2H2O(2分)
(4)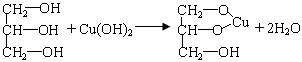 (2分)
(2分)
(5)不能 Al3+与F-反应生成配合物,且不与氨水发生反应,没有明显现象

 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案A.雷尼镍(Raney-Ni)是一种历史悠久、应用广泛的催化剂,由镍-铝合金为原料制得.
(1)元素第一电离能:Al
(2)雷尼镍催化的一实例为:
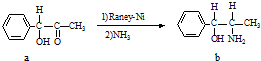 化合物b中进行sp
化合物b中进行sp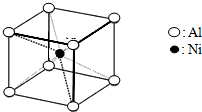 3杂化的原子有:
3杂化的原子有:(3)一种铝镍合金的结构如下图,与其结构相似的化合物是:
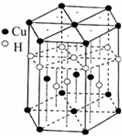
(4)实验室检验Ni2+可用丁二酮肟与之作用生成腥红色配合物沉淀.
①Ni2+在基态时,核外电子排布式为:
②在配合物中用化学键和氢键标出未画出的作用力(镍的配位数为

B.4-氯苯胺是合成橡胶、化学试剂、染料、色素等化工产品,制备4-氯苯胺的原理如下:
 .在1L密闭容器中加入4-氯硝基苯100g、雷尼镍(催化剂)及少量吗啉(脱氯抑制剂,
.在1L密闭容器中加入4-氯硝基苯100g、雷尼镍(催化剂)及少量吗啉(脱氯抑制剂,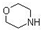 )、甲醇250mL(溶剂),密封;先充入氮气,然后充入氢气至一定压力.在所需氢气压力、温度等条件下加氢反应,充分反应后,冷却,过滤,洗涤,蒸馏并收集64~65℃馏分.
)、甲醇250mL(溶剂),密封;先充入氮气,然后充入氢气至一定压力.在所需氢气压力、温度等条件下加氢反应,充分反应后,冷却,过滤,洗涤,蒸馏并收集64~65℃馏分.(1)开始时先通入N2的目的是
(2)上述实验中过滤的目的是
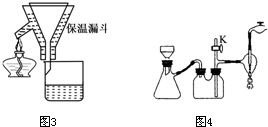
(3)蒸馏时除用到接引管、锥形瓶、温度计外,还用到的玻璃仪器有:
(4)以下是温度、氢气压力、催化剂用量及吗啉的用量对反应的影响.
| 表1温度 | 表2氢气压力 | 表3催化剂用量 | 表4吗啉用量 | |||||||||||||||
| 序号 | 温度/℃ | 转化率/% | 选择 性/% |
反应时间/h | 序号 | 氢气压力/MPa | 选择性/% | 反应时间/h | 序号 | 雷尼镍用量/g | 选择性/% | 反应时间/h | 序号 | 吗啉用量/% | 选择性/% | |||
| ① | 40 | 未完全 | 99.6 | 6 | ① | 0.5 | 99.6 | 3.7 | ① | 2 | 98.25 | 5 | ① | 0.0 | 84.3 | |||
| ② | 60 | 100 | 99.7 | 4 | ② | 1.0 | 99.7 | 2 | ② | 4 | 99.20 | 2.2 | ② | 0.3 | 99.3 | |||
| ③ | 80 | 100 | 99.6 | 2.45 | ③ | 1.5 | 99.2 | 1.6 | ③ | 6 | 99.60 | 1.9 | ③ | 0.5 | 99.7 | |||
| ④ | 100 | 100 | 99.6 | 2 | ④ | 2.0 | 96.4 | 1.15 | ④ | 8 | 99.60 | 1.4 | ④ | 0.7 | 99.6 | |||
| ⑤ | 120 | 100 | 98.6 | 1.7 | ⑤ | ⑤ | 10 | 99.10 | 1.4 | ⑤ | 1.2 | 99.7 | ||||||

 本题包括A、B两小题,分别对应于“物质结构与性质”和“实验化学”两个选修模块的内容.请选定其中一题,并在相应的答题区域内作答.若两题都做,则按A题评分.
本题包括A、B两小题,分别对应于“物质结构与性质”和“实验化学”两个选修模块的内容.请选定其中一题,并在相应的答题区域内作答.若两题都做,则按A题评分.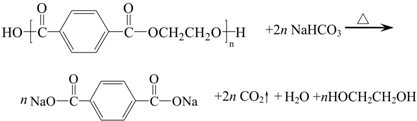
 本题包括A、B两小题,分别对应于“物质结构与性质”和“实验化学”两个选修模块的内容.请选定其中一题,并在相应和答题区域内作答.若两题都做,则按A题评分.
本题包括A、B两小题,分别对应于“物质结构与性质”和“实验化学”两个选修模块的内容.请选定其中一题,并在相应和答题区域内作答.若两题都做,则按A题评分.