题目内容
本题包括A、B两小题,分别对应于“物质结构与性质”和“实验化学”两个选修模块的内容.请选定其中一题,并在相应的答题区域内作答.若两题都做,则按A题评分.
A.《物质结构与性质》:原子序数依次增大的X、Y、Z、W四种元素,原子序数均小于36.已知X、Y和Z为第三周期元素,其原子的第一至第四电离能如下表:
(1)X、Y、Z的电负性从大到小的顺序为
(2)W元素应用广泛,是一种重要的生物金属元素,如人体内W元素的含量偏低,则会影响O2在体内的正常运输.已知W2+与KCN溶液反应得W(CN)2沉淀,当加入过量KCN溶液时沉淀溶解,生成配合物,其配离子结构如图所示.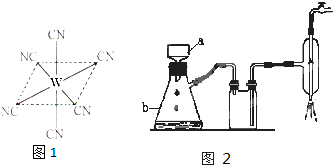
①W元素基态原子价电子排布式为
②已知CN-与
③上述沉淀溶解过程的化学方程式为
B.《化学实验》:无色晶体硫酸锌,俗称皓矾,在医疗上用作收敛剂,工业上作防腐剂、制造白色颜料(锌钡白)等.某实验小组欲用制氢废液制备硫酸锌晶体,进行了以下实验:
(1)取50mL制氢废液,过滤.除去不溶性杂质后,用ZnO调节滤液使pH约等于2,加热、蒸发、浓缩制得较高温度下的硫酸锌饱和溶液,冷却结晶,得到粗制的硫酸锌晶体.
①加入少量氧化锌调节滤液使pH≈2目的是
②加热蒸发、浓缩溶液时,应加热到
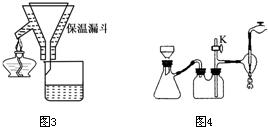
(2)粗晶体在烧杯中用适量蒸馏水溶解,滴加1~2滴稀硫酸,用沸水浴加热至晶体全部溶解.停止加热,让其自然冷却、结晶.抽滤(装置如图2所示).将所得晶体用少量无水乙醇洗涤1-2次,得到较纯的硫酸锌晶体.
①写出下列仪器的名称.a
②抽滤跟普通过滤相比,除了得到沉淀较干燥外,还有一个优点是
③用少量无水乙醇洗涤晶体的目的是
(3)在制取氢气时,如果锌粒中混有少量的铁、铜杂质,对硫酸锌的质量
A.《物质结构与性质》:原子序数依次增大的X、Y、Z、W四种元素,原子序数均小于36.已知X、Y和Z为第三周期元素,其原子的第一至第四电离能如下表:
| 电离能/kJ?mol-1 | I1 | I2 | I3 | I4 |
| X | 496 | 4562 | 6912 | 9543 |
| Y | 738 | 1451 | 7733 | 10540 |
| Z | 578 | 1817 | 2745 | 11578 |
Al>Mg>Na
Al>Mg>Na
(用元素符号表示),元素Y的第一电离能大于Z的原因是Y的最外层电子排布处于全满稳定状态,能量降低
Y的最外层电子排布处于全满稳定状态,能量降低
.(2)W元素应用广泛,是一种重要的生物金属元素,如人体内W元素的含量偏低,则会影响O2在体内的正常运输.已知W2+与KCN溶液反应得W(CN)2沉淀,当加入过量KCN溶液时沉淀溶解,生成配合物,其配离子结构如图所示.

①W元素基态原子价电子排布式为
3d64s2
3d64s2
.②已知CN-与
N2
N2
分子互为等电子体,1molCN-中π键数目为2NA
2NA
.③上述沉淀溶解过程的化学方程式为
Fe(CN)2+4KCN=K4[Fe(CN)6]
Fe(CN)2+4KCN=K4[Fe(CN)6]
.B.《化学实验》:无色晶体硫酸锌,俗称皓矾,在医疗上用作收敛剂,工业上作防腐剂、制造白色颜料(锌钡白)等.某实验小组欲用制氢废液制备硫酸锌晶体,进行了以下实验:
(1)取50mL制氢废液,过滤.除去不溶性杂质后,用ZnO调节滤液使pH约等于2,加热、蒸发、浓缩制得较高温度下的硫酸锌饱和溶液,冷却结晶,得到粗制的硫酸锌晶体.
①加入少量氧化锌调节滤液使pH≈2目的是
将硫酸转化成硫酸锌除去硫酸,且不带进其他杂质
将硫酸转化成硫酸锌除去硫酸,且不带进其他杂质
;②加热蒸发、浓缩溶液时,应加热到
溶液表面出现晶膜
溶液表面出现晶膜
时,停止加热.(2)粗晶体在烧杯中用适量蒸馏水溶解,滴加1~2滴稀硫酸,用沸水浴加热至晶体全部溶解.停止加热,让其自然冷却、结晶.抽滤(装置如图2所示).将所得晶体用少量无水乙醇洗涤1-2次,得到较纯的硫酸锌晶体.
①写出下列仪器的名称.a
布氏漏斗
布氏漏斗
;b吸滤瓶
吸滤瓶
.②抽滤跟普通过滤相比,除了得到沉淀较干燥外,还有一个优点是
过滤速度快
过滤速度快
.③用少量无水乙醇洗涤晶体的目的是
利用乙醇的挥发,除去晶体表面附着的水分,减少硫酸锌的损失
利用乙醇的挥发,除去晶体表面附着的水分,减少硫酸锌的损失
.(3)在制取氢气时,如果锌粒中混有少量的铁、铜杂质,对硫酸锌的质量
无
无
(填“有”、“无”)影响,原因是铜不与稀硫酸反应,过滤除去;铁虽然与稀硫酸反应生成硫酸亚铁,但锌比铁活泼,只要锌粒过量,就可置换硫酸亚铁中铁过滤除去
铜不与稀硫酸反应,过滤除去;铁虽然与稀硫酸反应生成硫酸亚铁,但锌比铁活泼,只要锌粒过量,就可置换硫酸亚铁中铁过滤除去
.分析:A、原子序数依次增大的X、Y、Z、W四种元素,原子序数均小于36,X、Y和Z为第三周期元素,由表中元素的电离能可知,X元素的第二电离能剧增,故X表现为+1价,故X为钠元素;Y的第三电离能剧增,Y为+2价,故Y为镁元素;Z的第四电离能剧增,表现+3价,故Y为铝元素.
(1)同周期自左而右,电负性增大,元素的第一电离能呈增大趋势,但能级处于半满、全满时,能量较低,元素的第一电离能高于同周期相邻元素.
(2)W元素应用广泛,是一种重要的生物金属元素,如人体内W元素的含量偏低,则会影响O2在体内的正常运输,可知W为Fe元素.
①Fe是26号元素,根据核外电子排布规律书写基态原子价电子排布式.
②原子总数相同,价层电子数相同的为等电子体.CN-中存在C≡N三键,三键中有1个σ键,2个π键,.
③由结构图可知Fe(CN)2与KCN反应生成K4[Fe(CN)6].
B、(1)①制氢气的废液中含有硫酸,应除去.
②加热至溶液表面出现晶膜时,停止加热,利用余热蒸干.
(2)①a是布氏漏斗,b是吸滤瓶.
②抽滤跟普通过滤相比,得到沉淀较干燥,过滤速度快.
③晶体表面附着水分.
(3)铜不与稀硫酸反应,过滤除去;铁虽然与稀硫酸反应生成硫酸亚铁,但锌比铁活泼,只要锌粒过量,就可置换硫酸亚铁中铁,过滤除去.
(1)同周期自左而右,电负性增大,元素的第一电离能呈增大趋势,但能级处于半满、全满时,能量较低,元素的第一电离能高于同周期相邻元素.
(2)W元素应用广泛,是一种重要的生物金属元素,如人体内W元素的含量偏低,则会影响O2在体内的正常运输,可知W为Fe元素.
①Fe是26号元素,根据核外电子排布规律书写基态原子价电子排布式.
②原子总数相同,价层电子数相同的为等电子体.CN-中存在C≡N三键,三键中有1个σ键,2个π键,.
③由结构图可知Fe(CN)2与KCN反应生成K4[Fe(CN)6].
B、(1)①制氢气的废液中含有硫酸,应除去.
②加热至溶液表面出现晶膜时,停止加热,利用余热蒸干.
(2)①a是布氏漏斗,b是吸滤瓶.
②抽滤跟普通过滤相比,得到沉淀较干燥,过滤速度快.
③晶体表面附着水分.
(3)铜不与稀硫酸反应,过滤除去;铁虽然与稀硫酸反应生成硫酸亚铁,但锌比铁活泼,只要锌粒过量,就可置换硫酸亚铁中铁,过滤除去.
解答:解:A、原子序数依次增大的X、Y、Z、W四种元素,原子序数均小于36,X、Y和Z为第三周期元素,由表中元素的电离能可知,X元素的第二电离能剧增,故X表现为+1价,故X为钠元素;Y的第三电离能剧增,Y为+2价,故Y为镁元素;Z的第四电离能剧增,表现+3价,故Y为铝元素.
(1)同周期自左而右,电负性增大,所以电负性从大到小的顺序为Al>Mg>Na;同周期自左而右,元素的第一电离能呈增大趋势,但Y的最外层电子排布处于全满稳定状态,能量降低,Y元素的第一电离能高于Z元素.
故答案为:Al>Mg>Na;Y的最外层电子排布处于全满稳定状态,能量降低.
(2)W元素应用广泛,是一种重要的生物金属元素,如人体内W元素的含量偏低,则会影响O2在体内的正常运输,可知W为Fe元素.
①Fe是26号元素,基态原子价电子排布式为3d64s2.
故答案为:3d64s2.
②将C原子及1个电子用“N”代换可得CN-等电子体分子N2;CN-中存在C≡N三键,三键中有1个σ键,2个π键,所以1molCN-中π键数目为2NA.
故答案为:N2;2NA.
③由结构图可知Fe(CN)2与KCN反应生成K4[Fe(CN)6],反应方程式为Fe(CN)2+4KCN=K4[Fe(CN)6].
故答案为:Fe(CN)2+4KCN=K4[Fe(CN)6].
B、(1)①制氢气的废液中含有硫酸,加入少量氧化锌,将硫酸转化成硫酸锌除去硫酸,且不带进其他杂质.
故答案为:将硫酸转化成硫酸锌除去硫酸,且不带进其他杂质.
②加热至溶液表面出现晶膜时,停止加热,利用余热蒸干.
故答案为:溶液表面出现晶膜.
(2)①a是布氏漏斗,b是吸滤瓶.
故答案为:布氏漏斗;吸滤瓶.
②抽滤跟普通过滤相比,不仅得到沉淀较干燥,而且过滤速度快.
故答案为:过滤速度快.
③晶体表面附着水分,硫酸锌不溶于酒精,利用乙醇的挥发,除去晶体表面附着的水分,减少硫酸锌的损失.
故答案为:利用乙醇的挥发,除去晶体表面附着的水分,减少硫酸锌的损失.
(3)铜不与稀硫酸反应,过滤除去;铁虽然与稀硫酸反应生成硫酸亚铁,但锌比铁活泼,只要锌粒过量,就可置换硫酸亚铁中铁,过滤除去,锌粒中混有少量的铁、铜杂质,对硫酸锌的质量无影响.
故答案为:无;铜不与稀硫酸反应,过滤除去;铁虽然与稀硫酸反应生成硫酸亚铁,但锌比铁活泼,只要锌粒过量,就可置换硫酸亚铁中铁过滤除去.
(1)同周期自左而右,电负性增大,所以电负性从大到小的顺序为Al>Mg>Na;同周期自左而右,元素的第一电离能呈增大趋势,但Y的最外层电子排布处于全满稳定状态,能量降低,Y元素的第一电离能高于Z元素.
故答案为:Al>Mg>Na;Y的最外层电子排布处于全满稳定状态,能量降低.
(2)W元素应用广泛,是一种重要的生物金属元素,如人体内W元素的含量偏低,则会影响O2在体内的正常运输,可知W为Fe元素.
①Fe是26号元素,基态原子价电子排布式为3d64s2.
故答案为:3d64s2.
②将C原子及1个电子用“N”代换可得CN-等电子体分子N2;CN-中存在C≡N三键,三键中有1个σ键,2个π键,所以1molCN-中π键数目为2NA.
故答案为:N2;2NA.
③由结构图可知Fe(CN)2与KCN反应生成K4[Fe(CN)6],反应方程式为Fe(CN)2+4KCN=K4[Fe(CN)6].
故答案为:Fe(CN)2+4KCN=K4[Fe(CN)6].
B、(1)①制氢气的废液中含有硫酸,加入少量氧化锌,将硫酸转化成硫酸锌除去硫酸,且不带进其他杂质.
故答案为:将硫酸转化成硫酸锌除去硫酸,且不带进其他杂质.
②加热至溶液表面出现晶膜时,停止加热,利用余热蒸干.
故答案为:溶液表面出现晶膜.
(2)①a是布氏漏斗,b是吸滤瓶.
故答案为:布氏漏斗;吸滤瓶.
②抽滤跟普通过滤相比,不仅得到沉淀较干燥,而且过滤速度快.
故答案为:过滤速度快.
③晶体表面附着水分,硫酸锌不溶于酒精,利用乙醇的挥发,除去晶体表面附着的水分,减少硫酸锌的损失.
故答案为:利用乙醇的挥发,除去晶体表面附着的水分,减少硫酸锌的损失.
(3)铜不与稀硫酸反应,过滤除去;铁虽然与稀硫酸反应生成硫酸亚铁,但锌比铁活泼,只要锌粒过量,就可置换硫酸亚铁中铁,过滤除去,锌粒中混有少量的铁、铜杂质,对硫酸锌的质量无影响.
故答案为:无;铜不与稀硫酸反应,过滤除去;铁虽然与稀硫酸反应生成硫酸亚铁,但锌比铁活泼,只要锌粒过量,就可置换硫酸亚铁中铁过滤除去.
点评:题目综合性较大,包含物质结构与化学实验,涉及电离能、电负性、核外电子排布规律、化学键与配合物、对实验利用的理解、实验条件控制、物质分离提纯等,难度较大,需要学生具备良好的心理素质、扎实的基础知识和运用知识理解问题的能力.

练习册系列答案
相关题目
本题包括A、B两小题,分别对应于“物质结构与性质”和“实验化学”两个选修模块的内容.请选定其中一题,并在相应的答题区域内作答.若两题都做,则按A题评分.
A.雷尼镍(Raney-Ni)是一种历史悠久、应用广泛的催化剂,由镍-铝合金为原料制得.
(1)元素第一电离能:Al Mg(选填:“>”、“<”、“=”)
(2)雷尼镍催化的一实例为: 化合物b中进行sp
化合物b中进行sp 3杂化的原子有: .
3杂化的原子有: .
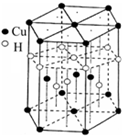
(3)一种铝镍合金的结构如下图,与其结构相似的化合物是: (选填序号:a.氯化钠 b.氯化铯 c.石英 d.金刚石).
(4)实验室检验Ni2+可用丁二酮肟与之作用生成腥红色配合物沉淀.
①Ni2+在基态时,核外电子排布式为: .
②在配合物中用化学键和氢键标出未画出的作用力(镍的配位数为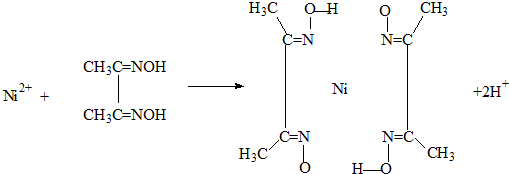
B.4-氯苯胺是合成橡胶、化学试剂、染料、色素等化工产品,制备4-氯苯胺的原理如下:
 .在1L密闭容器中加入4-氯硝基苯100g、雷尼镍(催化剂)及少量吗啉(脱氯抑制剂,
.在1L密闭容器中加入4-氯硝基苯100g、雷尼镍(催化剂)及少量吗啉(脱氯抑制剂, )、甲醇250mL(溶剂),密封;先充入氮气,然后充入氢气至一定压力.在所需氢气压力、温度等条件下加氢反应,充分反应后,冷却,过滤,洗涤,蒸馏并收集64~65℃馏分.
)、甲醇250mL(溶剂),密封;先充入氮气,然后充入氢气至一定压力.在所需氢气压力、温度等条件下加氢反应,充分反应后,冷却,过滤,洗涤,蒸馏并收集64~65℃馏分.
(1)开始时先通入N2的目的是 .
(2)上述实验中过滤的目的是 ,洗涤所用的试剂是 .
(3)蒸馏时除用到接引管、锥形瓶、温度计外,还用到的玻璃仪器有: 、 .馏出液的主要成分是 .
(4)以下是温度、氢气压力、催化剂用量及吗啉的用量对反应的影响.
优化的条件是:温度、氢气压力、催化剂用量、吗啉用量,选择的序号依次是 .
A.雷尼镍(Raney-Ni)是一种历史悠久、应用广泛的催化剂,由镍-铝合金为原料制得.
(1)元素第一电离能:Al
(2)雷尼镍催化的一实例为:
 化合物b中进行sp
化合物b中进行sp 3杂化的原子有:
3杂化的原子有:(3)一种铝镍合金的结构如下图,与其结构相似的化合物是:
(4)实验室检验Ni2+可用丁二酮肟与之作用生成腥红色配合物沉淀.
①Ni2+在基态时,核外电子排布式为:
②在配合物中用化学键和氢键标出未画出的作用力(镍的配位数为

B.4-氯苯胺是合成橡胶、化学试剂、染料、色素等化工产品,制备4-氯苯胺的原理如下:
 .在1L密闭容器中加入4-氯硝基苯100g、雷尼镍(催化剂)及少量吗啉(脱氯抑制剂,
.在1L密闭容器中加入4-氯硝基苯100g、雷尼镍(催化剂)及少量吗啉(脱氯抑制剂, )、甲醇250mL(溶剂),密封;先充入氮气,然后充入氢气至一定压力.在所需氢气压力、温度等条件下加氢反应,充分反应后,冷却,过滤,洗涤,蒸馏并收集64~65℃馏分.
)、甲醇250mL(溶剂),密封;先充入氮气,然后充入氢气至一定压力.在所需氢气压力、温度等条件下加氢反应,充分反应后,冷却,过滤,洗涤,蒸馏并收集64~65℃馏分.(1)开始时先通入N2的目的是
(2)上述实验中过滤的目的是
(3)蒸馏时除用到接引管、锥形瓶、温度计外,还用到的玻璃仪器有:
(4)以下是温度、氢气压力、催化剂用量及吗啉的用量对反应的影响.
| 表1温度 | 表2氢气压力 | 表3催化剂用量 | 表4吗啉用量 | |||||||||||||||
| 序号 | 温度/℃ | 转化率/% | 选择 性/% |
反应时间/h | 序号 | 氢气压力/MPa | 选择性/% | 反应时间/h | 序号 | 雷尼镍用量/g | 选择性/% | 反应时间/h | 序号 | 吗啉用量/% | 选择性/% | |||
| ① | 40 | 未完全 | 99.6 | 6 | ① | 0.5 | 99.6 | 3.7 | ① | 2 | 98.25 | 5 | ① | 0.0 | 84.3 | |||
| ② | 60 | 100 | 99.7 | 4 | ② | 1.0 | 99.7 | 2 | ② | 4 | 99.20 | 2.2 | ② | 0.3 | 99.3 | |||
| ③ | 80 | 100 | 99.6 | 2.45 | ③ | 1.5 | 99.2 | 1.6 | ③ | 6 | 99.60 | 1.9 | ③ | 0.5 | 99.7 | |||
| ④ | 100 | 100 | 99.6 | 2 | ④ | 2.0 | 96.4 | 1.15 | ④ | 8 | 99.60 | 1.4 | ④ | 0.7 | 99.6 | |||
| ⑤ | 120 | 100 | 98.6 | 1.7 | ⑤ | ⑤ | 10 | 99.10 | 1.4 | ⑤ | 1.2 | 99.7 | ||||||
 本题包括A、B两小题,分别对应于“物质结构与性质”和“实验化学”两个选修模块的内容.请选定其中一题,并在相应的答题区域内作答.若两题都做,则按A题评分.
本题包括A、B两小题,分别对应于“物质结构与性质”和“实验化学”两个选修模块的内容.请选定其中一题,并在相应的答题区域内作答.若两题都做,则按A题评分.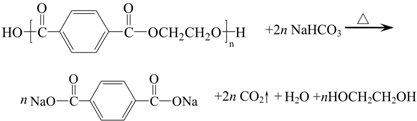
 本题包括A、B两小题,分别对应于“物质结构与性质”和“实验化学”两个选修模块的内容.请选定其中一题,并在相应和答题区域内作答.若两题都做,则按A题评分.
本题包括A、B两小题,分别对应于“物质结构与性质”和“实验化学”两个选修模块的内容.请选定其中一题,并在相应和答题区域内作答.若两题都做,则按A题评分.