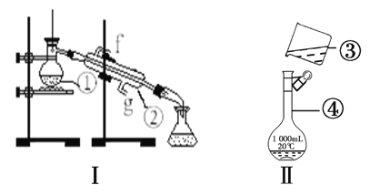
题目内容
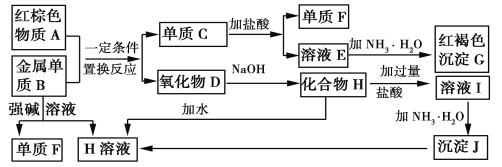
【题目】实验室用少量的溴和足量的乙醇制备1,2—二溴乙烷的装置如下图所示:
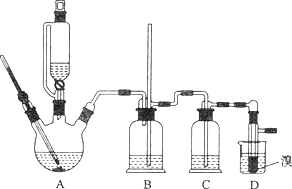
有关数据列表如下:
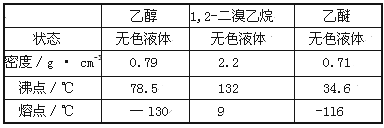
回答下列问题:
(1)写出该实验过程中发生的所有主要反应的化学方程式:________、_________。
(2)在此制各实验中,要尽可能迅速地把反应温度提高到170℃左右,其最主要目的是________(填正确选项前的字母,下同)。
a.引发反应 b.加快反应速度 c.防止乙醇挥发 d.减少副产物乙醚生成
(3)在装置C中应加入_______,其目的是吸收反应中可能生成的酸性气体。
a.水 b.浓硫酸 c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(4)判断该制备反应已经结束的最简单方法是______________(填实验现象)。
(5)将1,2-二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在_____层。
(6)若产物中有少量副产物乙醚,可用_______________的方法除去。
(7)反应过程中应用冷水冷却装置D,其主要目的是____________;但又不能过度冷却(如用冰水),其原因是__________________________。
【答案】 CH3CH2OH![]() CH2=CH2↑+H2O CH2=CH2+Br2→BrCH2CH2Br d c 溴的颜色完全褪去 下 蒸馏 避免溴大量挥发 产品1,2-二溴乙烷的熔点(凝固点)低,过度冷却会凝固而堵塞导管
CH2=CH2↑+H2O CH2=CH2+Br2→BrCH2CH2Br d c 溴的颜色完全褪去 下 蒸馏 避免溴大量挥发 产品1,2-二溴乙烷的熔点(凝固点)低,过度冷却会凝固而堵塞导管
【解析】分析:(1)乙醇在浓硫酸170℃的作用下生成乙烯,乙烯和溴水发生加成反应;
(2)乙醇在浓硫酸140℃的作用下发生分子间脱水;
(3)浓硫酸具有强氧化性,可能氧化乙醇中的碳;
(4)乙烯和溴水发生了加成反应;
(5)根据1,2-二溴乙烷和水的密度相对大小解答;
(6)利用1,2-二溴乙烷与乙醚的沸点不同进行解答;
(7)溴易挥发,该反应放热。
详解:(1)乙醇在浓硫酸170℃的条件下,发生消去反应生成乙烯,方程式为CH3CH2OH![]() CH2=CH2↑+H2O。乙烯和溴水发生加成反应生成1,2-二溴乙烷,方程式为CH2=CH2+Br2→BrCH2CH2Br;
CH2=CH2↑+H2O。乙烯和溴水发生加成反应生成1,2-二溴乙烷,方程式为CH2=CH2+Br2→BrCH2CH2Br;
(2)乙醇在浓硫酸140℃的条件下,发生分子内脱水,生成乙醚,所以要尽可能迅速地把反应温度提高到170℃左右,其最主要目的是减少副产物乙醚生成,答案选d;
(3)浓硫酸具有强氧化性,将乙醇氧化成二氧化碳,自身被还原成二氧化硫,二氧化碳、二氧化硫能和氢氧化钠溶液反应,答案选c;
(4)乙烯和溴水发生加成反应生成1,2-二溴乙烷,1,2-二溴乙烷为无色,所以判断该制备反应已经结束的最简单方法是溴的颜色完全褪去;
(5)1,2-二溴乙烷和水不互溶,1,2-二溴乙烷密度比水大,振荡后静置,产物应在下层;
(6)1,2-二溴乙烷与乙醚的沸点不同,两者均为有机物,互溶,用蒸馏的方法将它们分离;
(7)溴在常温下,易挥发,乙烯与溴反应时放热,溴更易挥发,冷却可避免溴的大量挥发,但1,2-二溴乙烷的凝固点9℃较低,不能过度冷却。