题目内容
(10分)按要求完成下列反应的化学方程式:
(1)碳和浓硫酸在加热条件下的反应:
;
(2)将氯气通入冷的消石灰中制取漂白粉:
;
(3)铝与NaOH溶液反应:
;
(4)在FeSO4溶液中加入NaOH溶液时,产生的白色絮状沉淀迅速变成灰绿色,最后变为红褐色。试写出上述变化的化学方程式:
。
(1)碳和浓硫酸在加热条件下的反应:
;
(2)将氯气通入冷的消石灰中制取漂白粉:
;
(3)铝与NaOH溶液反应:
;
(4)在FeSO4溶液中加入NaOH溶液时,产生的白色絮状沉淀迅速变成灰绿色,最后变为红褐色。试写出上述变化的化学方程式:
。
(每完成一个方程式给2分)
(1)C + 2H2SO4(浓)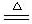 CO2↑+2SO2↑+2H2O
CO2↑+2SO2↑+2H2O
(2)2Cl2 + 2Ca(OH)2 ="=" CaCl2+Ca(ClO)2 +2 H2O
(3)2Al+2NaOH+2H2O=2NaAlO2+3H2↑
(4)FeSO4+2NaOH= Fe(OH)2↓+Na2SO4 4 Fe(OH)2 + O2 + 2H2O = 4Fe(OH)3
(1)C + 2H2SO4(浓)
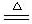 CO2↑+2SO2↑+2H2O
CO2↑+2SO2↑+2H2O(2)2Cl2 + 2Ca(OH)2 ="=" CaCl2+Ca(ClO)2 +2 H2O
(3)2Al+2NaOH+2H2O=2NaAlO2+3H2↑
(4)FeSO4+2NaOH= Fe(OH)2↓+Na2SO4 4 Fe(OH)2 + O2 + 2H2O = 4Fe(OH)3
考查常见方程式的书写。
(1)浓硫酸具有强氧化性,在加热的条件下能把碳以后生成CO2,方程式为C + 2H2SO4(浓)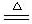 CO2↑+2SO2↑+2H2O。
CO2↑+2SO2↑+2H2O。
(2)漂白粉的主要成分是氯化钙和次氯酸钙,所以方程式为2Cl2 + 2Ca(OH)2 ="=" CaCl2+Ca(ClO)2 +2 H2O。
(3)铝和氢氧化钠溶液反应生成偏铝酸钠和氢气,方程式为
2Al+2NaOH+2H2O=2NaAlO2+3H2↑。
(4)氢氧化亚铁不稳定,在空气中易被以后生成氢氧化铁,方程式为FeSO4+2NaOH= Fe(OH)2↓+Na2SO4、4 Fe(OH)2 + O2 + 2H2O = 4Fe(OH)3。
(1)浓硫酸具有强氧化性,在加热的条件下能把碳以后生成CO2,方程式为C + 2H2SO4(浓)
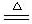 CO2↑+2SO2↑+2H2O。
CO2↑+2SO2↑+2H2O。(2)漂白粉的主要成分是氯化钙和次氯酸钙,所以方程式为2Cl2 + 2Ca(OH)2 ="=" CaCl2+Ca(ClO)2 +2 H2O。
(3)铝和氢氧化钠溶液反应生成偏铝酸钠和氢气,方程式为
2Al+2NaOH+2H2O=2NaAlO2+3H2↑。
(4)氢氧化亚铁不稳定,在空气中易被以后生成氢氧化铁,方程式为FeSO4+2NaOH= Fe(OH)2↓+Na2SO4、4 Fe(OH)2 + O2 + 2H2O = 4Fe(OH)3。

练习册系列答案
相关题目
