题目内容
【题目】在不同条件下,分别测得反应2SO2(g)+O2(g)2SO3(g)的速率如下,其中化学反应速率最快的是( )
A. v(SO2)=4 mol·L-1·min-1 B. v(O2)=2 mol·L-1·min-1
C. v(SO3)=6 mol·L-1·min-1 D. v(O2)=1 mol·L-1·min-1
【答案】C
【解析】根据反应速率之比是相应的化学计量数之比可知如果都用SO2表示该反应速率,则分别是( mol·L-1·min-1)4、4、6、2,所以反应速率最快的是选项C,答案选C。

 每课必练系列答案
每课必练系列答案 巧学巧练系列答案
巧学巧练系列答案【题目】实验室利用废铜合金(含少量铁和铝)来制取硫酸铜晶体(CuSO4·5H2O),方案如下:

金属离子生成氢氧化物沉淀的pH可参考下列数据:
Fe3+ | Fe2+ | Cu2+ | Al3+ | |
开始沉淀时的pH | 2.2 | 7.5 | 5.2 | 3.7 |
完全沉淀时的pH | 3.2 | 9.0 | 6.7 | 4.7 |
请回答:
(1)若溶解合金时加入的混酸由2 L 3 mol·L-1硫酸和1 L 2 mol·L-1硝酸混合而成,则反应后生成标准状况下的NO的体积最多为____________L。
(2)加入H2O2的目的是____________。
(3)为保证产品的纯度,M物质最好选用________(填字母),调节pH的范围为____________。
a.Cu(OH)2 b.H2SO4 c.NH3·H2O d.Na2CO3
(4)滤液D中加入硫酸的目的为_______________________________________。
(5)从溶液E制得CuSO4·5H2O晶体所需要的步骤为________、结晶、过滤和干燥。
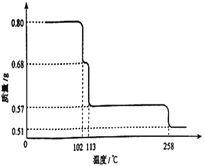
(6)0.80g CuSO4·5H2O样品受热脱水过程的热重曲线(样品质量随温度变化的曲线)如图所示。试确定200℃时固体物质的化学式______________。