��Ŀ����
����Ŀ�����ڷ�ӦN2O4(g)![]() 2NO2(g)���¶�һ��ʱ��ƽ����ϵ��NO2�����������(NO2)��ѹǿ�ı仯�����ͼ��ʾ��ʵ���ϵ��κ�һ��Ϊ��Ӧѹǿ�µ�ƽ��㣩������˵����ȷ����
2NO2(g)���¶�һ��ʱ��ƽ����ϵ��NO2�����������(NO2)��ѹǿ�ı仯�����ͼ��ʾ��ʵ���ϵ��κ�һ��Ϊ��Ӧѹǿ�µ�ƽ��㣩������˵����ȷ����
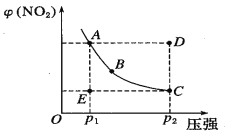
A. A��C���������Ӧ���ʵĹ�ϵΪA��C
B. A��B��C��D��E��״̬�У�v(��)��v(��)����״̬E
C. ά��P1���䣬E��A����ʱ��Ϊx��ά��P2���䣬D��C����ʱ��Ϊy����x��y
D. ʹE״̬��ˮƽ����C״̬����������������ѡ�õ������Ǵ�P1ͻȻ��ѹ��P2
���𰸡�D
��������
A.����������μӵĻ�ѧ��Ӧ������ѹǿ����ѧ��Ӧ������������C���Ӧ��ѹǿ����A���ѹǿ����������Ӧ����vA��vC��A����
B.��ͼ���У�A��B��C���㶼��ƽ�����ϣ���������������淴Ӧ������ȣ�E��Ҫ�ﵽƽ�⣬�������NO2������������Ҳ���Ƿ�ӦҪ������Ӧ������У��Ӷ��ó�v(��)��v(��)�� B����
C.����ѹǿ����ѧ��Ӧ������������D���ѹǿ����E���ѹǿ������D��ķ�Ӧ���ʴ���E��ķ�Ӧ���ʣ�������ʱ��x��y��C����
D.�����ټ�ѹʱ��ƽ��δ�ƶ�����������ѹʱ��ƽ�ⲻ�ϵر��ƻ������ֲ��ϵؽ����µ�ƽ�⣬������ʹE״̬��ˮƽ����C״̬����ӦͻȻ��ѹ������C��ƽ�������Դ�A״̬����Ӧ������ѹ��D��ȷ��
�ʺ���ѡ����D��

����Ŀ����֪��Ӧ![]() ��ij�о�С�齫4moX��2molY����һ�ݻ�������ܱ������У��ⶨһ��ʱ����X��ת���ʣ��õ������������ʾ�������ж���ȷ���ǣ� ��
��ij�о�С�齫4moX��2molY����һ�ݻ�������ܱ������У��ⶨһ��ʱ����X��ת���ʣ��õ������������ʾ�������ж���ȷ���ǣ� ��
t/min | 2 | 4.5 | 5 | 6 |
X��ת���� | 30% | 40% | 70% | 70% |
A.���ŷ�Ӧ�Ľ��У����������ܶȲ�������
B.��Ӧ��5.5minʱ��v����X��=2v����Z��
C.6minʱ��������ʣ��1.4molY
D.�����������䣬��X�����ʵ�����Ϊ10mol����ɵõ�4molZ