题目内容
可逆反应N2(g)+ 3H2(g) 
 2NH3 (g)达到平衡状态,下列说法中正确的是( )
2NH3 (g)达到平衡状态,下列说法中正确的是( )
| A.该反应停止,N2和H2不再化合 | B.N2、H2、NH3浓度不变 |
| C.N2、H2、NH3浓度相等 | D.N2、H2、NH3的物质的量之比为1:3:2 |
B
解析试题分析:当可逆反应达到平衡状态时,反应仍然在进行,只是任何物质的消耗浓度与产生浓度相等,即浓度不发生变化,因此选项A错误,选项B正确;当反应达到平衡时N2、H2、NH3浓度可能相等,也可能不等,这与开始投入的物质的量的多少有关,选项C错误; D. N2、H2、NH3的物质的量改变之比为1:3:2,但是平衡时的浓度之比比一定是该数值,因此选项D错误。
考点:考查可逆反应平衡状态的特征及浓度、物质的量的关系的知识。

练习册系列答案
相关题目
在一定温度下的恒容密闭容器中,当下列哪些物理量不再发生变化时,表明下述反应A(s)+2B(g)  C(g)+D(g)已达到平衡状态①各气体物质的物质的量浓度②气体的总物质的量③混合气体的压强④混合气体的密度
C(g)+D(g)已达到平衡状态①各气体物质的物质的量浓度②气体的总物质的量③混合气体的压强④混合气体的密度
| A.只有①② | B.只有①④ | C.只有①③④ | D.①②③④ |
升高温度,下列数据不一定增大的是
A.化学反应速率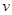 | B.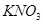 的溶解度S 的溶解度S |
| C.化学平衡常数K | D.水的离子积常数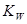 |
一定条件下,在容积为10L的密闭容器中,将l mol X和1 mol Y进行如下反应:
2X(g)+Y(g)  Z(g),经60 s达到平衡生成0.3 mol的Z,下列说法正确的是( )
Z(g),经60 s达到平衡生成0.3 mol的Z,下列说法正确的是( )
| A.60 s内X的平均反应速率为0.001 mol·L-1·s-1 |
| B.将容器的容积变为20 L,Z的新平衡浓度将等于原平衡浓度的1/2 |
| C.若温度和体积不变,往容器内增加1 mol X,Y的转化率将增大 |
| D.若升高温度,X的体积分数增大,则正反应的△H>0 |
决定化学反应速率的主要因素是
| A.反应物的浓度 | B.反应温度 | C.使用催化剂 | D.反应物的性质 |
科学家一直致力于“人工固氮”的新方法研究。目前合成氨技术原理为:
N2(g) + 3H2(g) 2NH3(g);△H=—92.4kJ·mol—1。在673K,30MPa下,上述合成氨反应中n(NH3)和n(H2)随时间变化的关系如图所示。下列叙述正确的是( )
2NH3(g);△H=—92.4kJ·mol—1。在673K,30MPa下,上述合成氨反应中n(NH3)和n(H2)随时间变化的关系如图所示。下列叙述正确的是( )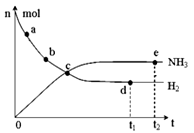
| A.点a的正反应速率比点b的大 |
| B.点c处反应达到化学平衡状态 |
| C.点d和点e处的n(N2)不相同 |
| D.点e反应达到化学平衡状态,反应停止 |
在t℃时,10mL0.4mol·L-1H2O2溶液发生催化分解:2H2O2 = 2H2O + O2↑,不同时刻测得生成O2的体积(已折算为标准状况)如下表
| t /min | 0 | 2 | 4 | 6 |
| V(O2)/mL | 0.0 | 9.9 | 17.2 | 22.4 |
A.0~2min H2O2平均反应速率比4~6min快
B.0~6min的平均反应速率 v(H2O2)≈3.3×10-2mol·L-1·min-1
C.反应至6min时,c(H2O2)=0.3mol·L-1
D.反应至6min时,H2O2分解了50%
下列事实不能用勒夏特列原理解释的是 ( )
| A.工业生产硫酸的过程中使用过量的氧气,以提高二氧化硫的转化率 |
| B.合成氨工厂通常采用20MPa~50MPa压强,以提高原料的利用率; |
| C.过氧化氢分解加二氧化锰作催化剂,使单位时间内产生的氧气的量多。 |
| D.久制的氯水PH值变小。 |
 2AB(g),达到平衡的标志是
2AB(g),达到平衡的标志是