题目内容
【题目】铁、铜及其化合物在工农业生产中应用广泛。
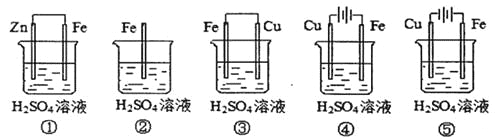
(1)在潮湿空气中,钢铁发生电化学腐蚀转化为Fe(OH)2的反应方程式为_______。在含有等浓度硫酸溶液的下列装置中,铁腐蚀的速率由快到慢的顺序是____________(用序号填写)。
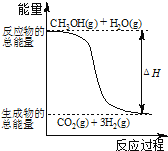
(2)已知:①3Fe(s)+2O2(g)=Fe3O4(s)![]() H=-1118 kJ·mol-1
H=-1118 kJ·mol-1
②2Al(s)+3/2O2(g)=A12O3(s)![]() H=-1675.7 kJ·mol-1
H=-1675.7 kJ·mol-1
则焊接钢轨时铝与Fe3O4发生反应生成铁和Al2O3的热化学方程式为______________。
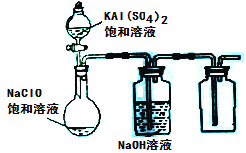
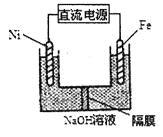
(3)Na2FeO4具有强氧化性,其电解制法如图所示,请写出阳极的电极反应式______。Na2FeO4是一种既能杀菌、消毒,又能絮凝净水的水处理剂,其原理是______________。
(4)工业上常用FeCl3溶液腐蚀印刷线路板,发生反应的离子方程式是____________。若腐蚀铜板后的溶液中,Cu2+、Fe3+和Fe2+浓度均为0.1 mol·L-1,结合下图分析,当混合溶液中通入氨气调节溶液的pH=5.6时,溶液中存在的金属阳离子为____。从图中数据计算Fe(OH)2的溶度积Ksp[Fe(OH)2]=______。
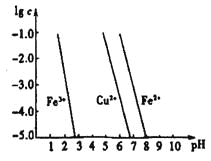
已知:横坐标为溶液的pH,纵坐标为金属离子的物质的量浓度的对数(当溶液中金属离子浓度![]() 10-5mol·L-1时,可认为沉淀完全)。
10-5mol·L-1时,可认为沉淀完全)。
【答案】2Fe + O2+ 2H2O = 2Fe(OH)2 ⑤③②①④ 8Al(s)+3Fe3O4(s)=4Al2O3(s)+9Fe(s) △H= 3349.8 kJ·mol-1 Fe + 8OH--6e-= FeO42-+ 4H2O Na2FeO4具有强氧化性,能起到杀菌、消毒作用;高价的铁被还原成的Fe3+水解生成Fe(OH)3胶体,能吸附水中杂质。 2Fe3+ + Cu = 2Fe2++Cu2+ Cu2+、Fe2+ 1.0×10-17(mol·L-1)3
【解析】
(1)在潮湿空气中,钢铁发生电化学腐蚀转化为Fe(OH)2的反应方程式为: 2Fe + O2+ 2H2O = 2Fe(OH)2;①Zn为负极,Fe为正极,Fe受到保护;②Fe与硫酸发生置换反应,被氧化变为Fe2+,比①腐蚀的快;③构成Fe-Cu原电池,Fe作负极,首先被腐蚀,腐蚀速率③>②;④形成电解池,Fe为阴极,被保护,只要存在外加电源,Fe就不会被腐蚀,所以腐蚀速率④<①;⑤构成电解池。由于Fe为阳极,被氧化,发生氧化反应,腐蚀速率比③快。所以铁腐蚀的速率由快到慢的顺序是⑤③②①④;
(2)②×4-①×3,整理可得:8Al(s)+3Fe3O4(s)=4Al2O3(s)+9Fe(s) △H= 3349.8 kJ·mol-1;(3)Na2FeO4具有强氧化性,其电解制法如图所示,则在阳极,Fe失去电子,被氧化,与溶液中的OH-结合反应,阳极的电极反应式是Fe + 8OH--6e-= FeO42-+ 4H2O;Na2FeO4是一种既能杀菌、消毒,又能絮凝净水的水处理剂,其原理是Na2FeO4中的Fe化合价为+6价,具有强氧化性,能起到杀菌、消毒作用;高价的铁被还原成的Fe3+发生水解反应生成Fe(OH)3胶体,表面积大,吸附能力强,能吸附水中杂质,使之形成沉淀,从水中分离出去,从而使水得到净化。(4)工业上常用FeCl3溶液腐蚀印刷线路板,Fe3+将Cu单质氧化为Cu2+,Fe3+被还原变为Fe2+,根据电子守恒、电荷守恒及原子守恒,可得发生反应的离子方程式是2Fe3+ + Cu = 2Fe2++Cu2+;根据图像可知,在溶液的pH接近3而小于3时,Fe3+已经沉淀完全。所以在溶液的pH=5.6时,溶液中存在的金属阳离子为Cu2+、Fe2+;Fe(OH)2的溶度积Ksp[Fe(OH)2]=c(Fe2+)c2(OH-)=10-5×(10-14÷10-8)21.0×10-17(mol·L-1)3。

 ABC考王全优卷系列答案
ABC考王全优卷系列答案【题目】CCuS是一种二氧化碳的捕获、利用与封存的技术,这种技术可将CO2资源化, 产生经济效益。CO2经催化加氢可以生成低碳有机物,主要有以下反应:
反应I:CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g) △H1=-49.8kJ·mol-1
CH3OH(g)+H2O(g) △H1=-49.8kJ·mol-1
反应II:CH3OCH3(g)+H2O(g) ![]() 2CH3OH(g) △H2=+23.4kJ·mol-1
2CH3OH(g) △H2=+23.4kJ·mol-1
反应III:2CO2(g)+6H2(g) ![]() CH3OCH3(g)+3H2O(g) △H3
CH3OCH3(g)+3H2O(g) △H3
(1)△H3=_____________kJ·mol-1
(2)恒温恒容条件下,在密闭容器中通人等物质的量的CO2和H2,发生反应I。下列描述能说明反应I达到平衡状态的是_______(填序号)。
A.容器内的混合气体的密度保持不变B.反应体系总压强保持不变
C.CH3OH和CO2的浓度之比保持不变D.断裂3NA个H-O键同时断裂2NA个C=O键
(3)反应II在某温度下的平衡常数为0.25,此温度下,在密闭容器中加人等物质的量的 CH3OCH3(g)和H2O(g),反应到某时刻测得各组分浓度如下:
物质 | CH3OCH3(g) | H2O(g) | CH3OH(g) |
浓度/mol·L-1 | 1.6 | 1.6 | 0.8 |
此时![]() ___
___![]() (填“>”、“<”或“=”),当反应达到平衡状态时,混合气体中CH3OH 体积分数 V(CH3OH)%= _____%。
(填“>”、“<”或“=”),当反应达到平衡状态时,混合气体中CH3OH 体积分数 V(CH3OH)%= _____%。
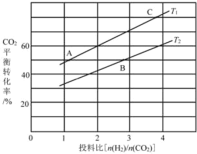
(4)在某压强下,反应III在不同温度、不同投料比时,CO2的平衡转化率如图所示。T1温度下,将6 mol CO2和12 mol H2充入3 L的密闭容器中,10 min后反应达到平衡状态,则0-10 min内的平均反应速率V(CH3OCH3)=____。
(5)恒压下将CO2和氏按体积比1 :3混合,在 不同催化剂作用下发生反应I和反应III,在相同的时间段内CH3OH的选择性和产率随温度的变化如下图。
其中:CH3OH的选择性=![]() ×100%
×100%
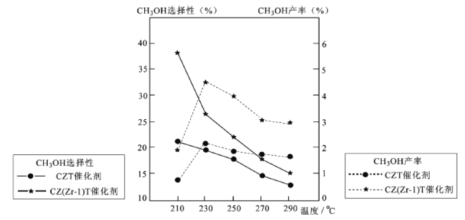
②在上述条件下合成甲醇的工业条件是_________。
A. 230℃ B. 210℃ C.催化剂 CZT D.催化剂 CZ(Zr-1)T