��Ŀ����
16����ϩ�ڻ��������е���;�㷺��������������ϩ�ǹ�ҵ�ϳ��÷���������������ϩ�IJ���һֱ�ǿ�ѧ���о��ķ����ֽ�CO2����������������ϩ���о��ڹ�����ѧ��������ϴ��ע����Ҫ�漰���·�Ӧ����Ӧ�٣�C2H6?C2H4+H2 ��H1
��Ӧ�ڣ�CO2+H2?CO+H2O��g�� H2��0
�ܷ�Ӧ�ۣ�C2H6+CO2?C2H4+H2O��g��+CO��H3
��1����Ӧ�ٵġ�S��0�������������
��2���ڹ�ҵ�����У�Ϊ����߷�Ӧ������ϩ�IJ��ʣ����������O2��ȥ���ɵ�H2���Խ��Ͳ�ȡ��һ��ʩ��ԭ����������������Ӧ����ˮ������������Ũ�ȣ���Ӧ��ƽ�������ƶ��������ϩ�IJ��ʣ�������O2��������ǿ����ϩ�����ᱻ������������ϩ�IJ�����߲�����ʵ�����壮
��3�����й��ڸ��о���˵����ȷ���ǣ�BD����д��Ӧ�ı�ţ�
A��Ϊ�ӿ췴Ӧ���ʣ�������ʵ���¶�Խ��Խ�ã������ÿ��IJ������Ӷ���߾���Ч�棻
B���о��������ʵĴ������ӿ췴Ӧ���ʣ�
C������CO2�ɼӿ췴Ӧ�ٵ����ʣ��Ӷ������ϩ�IJ��ʣ�
D������CO2�Է�Ӧ�ٵĸ�������ϡ�͵����ã��ں�ѹ�����¿���������ת���ʣ�
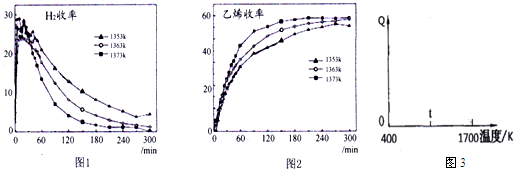
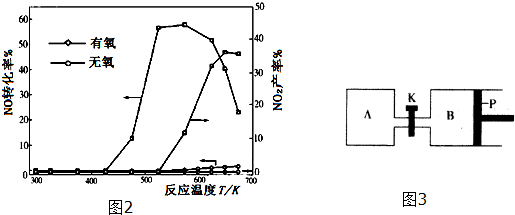
��4��Ϊ�о��¶ȶ���ϩ���ʵ�Ӱ�죬ʵ���ͼ1��ͼ2���Է���ͼ1 ��H2������ͬһ�¶�����ʱ��仯���½���ԭ��Ӧ���ж�����̼����������ʹ���������ʽ��ͣ���ͼ2�з�����Ӧ�۵ġ�H3��0�������������
��5��д����Ӧ�ڵ�ƽ�ⳣ������ʽ��K=$\frac{c��CO����c��{H}_{2}O��}{c��C{O}_{2}����c��{H}_{2}��}$������Ũ����Q=$\frac{������Ũ�ȵ�ϵ���η��ij˻�}{��Ӧ��Ũ�ȵ�ϵ���η��ij˻�}$��400Kʱ���ڹ̶�������ܱ������У��������ʵ���Ϊ1��1��CO2��H2������һ��ʱ��t��ƽ�⣬�������¶���1700K����ͼ3������Ӧ�����¶�����ʱQֵ�ı仯����ͼ��
���� ��1����Ӧ��Ϊ�������ʵ�������Ӧ�����Ҷ�����
��2��������������Ӧ����ˮ������������Ũ�ȣ�ʹƽ�������ƶ���
��3��A���¶ȷdz��ߣ���Ҫ�ṩ�϶�����������豸Ҫ��Ҳ�ܸߣ���������ۺϾ���Ч�棻
B���о��������ʵĴ������ӿ췴Ӧ���ʣ���߾���Ч�棻
C������CO2ʹ��Ӧ��������Ũ�Ƚ��ͣ���Ӧ���ʼ�����
D���ں�ѹ�����¼���CO2�Է�Ӧ�ٵĸ�������ϡ�͵����ã�ƽ�������ƶ���
��4����ͼ1��֪����Ӧ���ж�����̼����������ʹ���������ʽ��ͣ�
��ͼ2��֪�����¶����ߣ���ϩ����������˵�������¶�ƽ��������Ӧ�����ƶ���
��5��ƽ�ⳣ����ָ������ƽ��Ũ�Ȼ�ѧ�������ݳ˻��뷴Ӧ��Ũ�Ȼ�ѧ�������ݳ˻��ıȣ�
δ����ƽ��ǰ��������Ũ������Ӧ��Ũ�ȼ�С����Qֵ��С������ƽ��ʱ�������¶ȣ�ƽ�������ƶ���Qֵ��С��
��� �⣺��1����Ӧ��Ϊ�������ʵ�������Ӧ�����Ҷ����ʡ�S��0���ʴ�Ϊ������
��2��������������Ӧ����ˮ������������Ũ�ȣ���Ӧ��ƽ�������ƶ�����߷�Ӧ������ϩ�IJ��ʣ�
�ʴ�Ϊ��������������Ӧ����ˮ������������Ũ�ȣ���Ӧ��ƽ�������ƶ��������ϩ�IJ��ʣ�
��3��A���¶ȷdz��ߣ���Ҫ�ṩ�϶�����������豸Ҫ��Ҳ�ܸߣ���������ۺϾ���Ч�棬��A����
B���о��������ʵĴ������ӿ췴Ӧ���ʣ���߾���Ч�棬��B��ȷ��
C������CO2ʹ��Ӧ��������Ũ�Ƚ��ͣ�����ͨ����ϩ����������Ӧ���ʼ�������C����
D���ں�ѹ�����¼���CO2�Է�Ӧ�ٵĸ�������ϡ�͵����ã�ƽ�������ƶ�������������ת���ʣ���D��ȷ��
��ѡ��BD��
��4����ͼ1��֪����Ӧ���ж�����̼����������ʹ���������ʽ��ͣ�
��ͼ2��֪�����¶����ߣ���ϩ����������˵�������¶�ƽ��������Ӧ�����ƶ�������ӦΪ���ȷ�Ӧ����Ӧ�۵ġ�H3��0��
�ʴ�Ϊ����Ӧ���ж�����̼����������ʹ���������ʽ��ͣ�����
��5����Ӧ�ڵ�ƽ�ⳣ������ʽK=$\frac{c��CO����c��{H}_{2}O��}{c��C{O}_{2}����c��{H}_{2}��}$��δ����ƽ��ǰ��������Ũ������Ӧ��Ũ�ȼ�С����Qֵ��С������ƽ��ʱ�������¶ȣ�ƽ�������ƶ���Qֵ��С����Ӧ�����¶�����ʱQֵ�ı仯����ͼΪ�� ��
��
�ʴ�Ϊ��$\frac{c��CO����c��{H}_{2}O��}{c��C{O}_{2}����c��{H}_{2}��}$�� ��
��
���� ���⿼�黯ѧƽ��Ӱ�����ء�ƽ�ⳣ���ȣ�ע��Ի���֪ʶ���������գ��Ѷ��еȣ�

 ����������������ϵ�д�
����������������ϵ�д�| A�� | NaCl��CaCO3 | B�� | CaCO3��Cl2 | C�� | Cl2��Ca��OH��2 | D�� | Ca��OH��2��NaCl |
 ʵ�����Ʊ�1��2-��������ķ�Ӧԭ�����£�
ʵ�����Ʊ�1��2-��������ķ�Ӧԭ�����£�CH3CH2OH$��_{170��}^{H_{2}SO_{4}��Ũ��}$CH2=CH2
CH2=CH2+Br2��BrCH2CH2Br
���ܴ��ڵ���Ҫ����Ӧ�У��Ҵ���Ũ����Ĵ�������l40����ˮ�������ѣ�
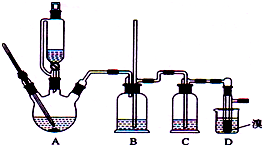
������������������Ҵ��Ʊ�1��2-���������װ����ͼ��ʾ��
�й������б����£�
| �Ҵ� | 1��2-�������� | ���� | |
| ״̬ | ��ɫҺ�� | ��ɫҺ�� | ��ɫҺ�� |
| �ܶ�/g•cm-3 | 0.79 | 2.2 | 0.71 |
| �е�/�� | 78.5 | 132 | 34.6 |
| �۵�/�� | һl30 | 9 | -1l6 |
��1���ڴ��Ƹ�ʵ���У�Ҫ������Ѹ�ٵذѷ�Ӧ�¶���ߵ�170�����ң�������ҪĿ����d��������ȷѡ��ǰ����ĸ��
a��������Ӧ b���ӿ췴Ӧ�ٶ� c����ֹ�Ҵ��ӷ� d�����ٸ�������������
��2����װ��C��Ӧ����c����Ŀ�������շ�Ӧ�п������ɵ��������壺������ȷѡ��ǰ����ĸ��
a��ˮ b��Ũ���� c������������Һ d������̼��������Һ
��3�������������������������ѣ���������ķ�����ȥ��
��4����Ӧ������Ӧ����ˮ��ȴװ��D������ҪĿ���DZ���������ӷ������ֲ��ܹ�����ȴ�����ñ�ˮ������ԭ���Dz�Ʒ1��2-����������۵㣨���̵㣩�ͣ�������ȴ�����̶��������ܣ�
�������������Դ�������ȷ������Ź㷺����;��ʪ�����ɷ��Ʊ��������ε�ԭ�����±���ʾ��
| ʪ�� | ǿ���Խ����У�Fe��NO3��3��NaClO��Ӧ�����Ϻ�ɫ����������Һ |
| �ɷ� | Fe2O3��KNO3��KOH��ϼ��ȹ��������Ϻ�ɫ�������κ�KNO2�Ȳ��� |
�ٷ�ӦI�Ļ�ѧ����ʽΪ2NaOH+Cl2�TNaCl+NaClO+H2O��
�ڷ�ӦII�����ӷ���ʽΪ3ClO-+10OH-+2Fe3+=2FeO42-+3Cl-+5H2O��
����֪25��ʱFe��OH��3��Ksp=4.0��10-38����ӦII����Һ��c��Fe3+��=4��10-5mol•L-1����Fe3+��ȫ����ʱ��pH=3��
��2�����������һ�������ˮ���������䴦��ˮ��ԭ��Ϊ���������ǿ�����ԣ���ɱ����������ˮ�б���ԭ����Fe��OH��3���塢����������ˮ���ã�
��3���ɷ��Ʊ�K2FeO4�ķ�Ӧ���������뻹ԭ�������ʵ���֮��Ϊ3�s1��
��4��������������������еĿɳ��ɵ�أ�ͼ2Ϊ�õ�غͳ��õĸ��ܼ��Ե�صķŵ����ߣ��ɴ˿ɵó��ĸ�����ص��ŵ��зŵ�ʱ�䳤��������ѹ�ȶ���


 +Br2$\stackrel{Fe}{��}$
+Br2$\stackrel{Fe}{��}$ +HBr��
+HBr��
 ��̼���ƣ�Na2CO4����ϴ�ӡ�ӡȾ����֯����ֽ��ҽҩ�����������д���Ӧ�ã�
��̼���ƣ�Na2CO4����ϴ�ӡ�ӡȾ����֯����ֽ��ҽҩ�����������д���Ӧ�ã�