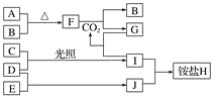
ЬтФПФкШн
ЁОЬтФПЁПЖЌМОЪЧЮэіВЬьЦјИпЗЂЕФМОНкЃЌЦфжаЦћГЕЮВЦјКЭШМУКЮВЦјЪЧдьГЩЮэіВЕФдвђжЎвЛЁЃ
ЃЈ1ЃЉЪЙгУМзДМЦћгЭПЩвдМѕЩйЦћГЕЮВЦјЖдЛЗОГЕФЮлШОЁЃЙЄвЕЩЯдк200ЁцКЭ10MPaЕФЬѕМўЯТПЩгУМзЭщКЭбѕЦјЭЈЙ§ЭжЦЙмЕРЗДгІжЦЕУМзДМЃЌвбжЊвЛЖЈЬѕМўЯТЃЌCH4КЭCH3OHЕФШМЩеШШЗжБ№784kJ/molКЭ628kJ/molдђ2CH4(g)+O2(g)=2CH3OH(g) ЁїH=___ЁЃ
ЃЈ2ЃЉЖўМзУбвВЪЧЧхНрФмдДЁЃгУКЯГЩЦјдкДпЛЏМСДцдкЯТжЦБИЖўМзУбЕФЗДгІдРэЮЊЃК2CO(g)+4H2(g)CH3OCH3(g) +H2O(g) ЁїH<0ЁЃ
ЂйФГЮТЖШЯТЃЌНЋ2.0molCO(g)КЭ6.0molH2(g)ГфШыШнЛ§ЮЊ2LЕФУмБеШнЦїжаЃЌЗДгІЕНДяЦНКтЪБЃЌИФБфбЙЧПКЭЮТЖШЃЌЦНКтЬхЯЕжаCH3OCH3(g)ЕФЮяжЪЕФСПЗжЪ§БфЛЏЧщПіШчЭМЫљЪОЃЌЙигкЮТЖШКЭбЙЧПЕФЙиЯЕХаЖЯе§ШЗЕФЪЧ____ЁЃ

A.P3>P2ЃЌT3>T2
B.P1>P3ЃЌT1>T3
C.P1>P4ЃЌT2>T3
D.P2>P4ЃЌT4>T2
ЂкдкКуШнУмБеШнЦїРяАДЬхЛ§БШЮЊ1ЃК3ГфШывЛбѕЛЏЬМКЭЧт ЦјЃЌвЛЖЈЬѕМўЯТЗДгІДяЕНЦНКтзДЬЌЃЎЕБИФБфЗДгІЕФФГвЛИіЬѕМўКѓЃЌЯТСаБфЛЏФмЫЕУїЦНКтвЛЖЈЯђФцЗДгІЗНЯђвЦЖЏЕФЪЧ___ЁЃ
A.ЧтЦјЕФзЊЛЏТЪМѕаЁ B.ФцЗДгІЫйТЪЯШдіДѓКѓМѕаЁ
C.ЛЏбЇЦНКтГЃЪ§KжЕдіДѓ D.ЗДгІЮяЕФЬхЛ§АйЗжКЌСПдіДѓ
ЃЈ3ЃЉЦћГЕЮВЦјОЛЛЏЕФжївЊдРэЮЊЃК2NO(g)+2CO(g)![]() 2CO2(g) +N2(g)
2CO2(g) +N2(g)
Ђй200KЁЂpPaЪБЃЌдквЛИіШнЛ§ЮЊ2LЕФКуЮТУмБеШнЦїжаГфШы1.5molNOКЭ2.0molCOЃЌПЊЪМЗДгІжС2minЪБВтЕУCOзЊЛЏТЪЮЊ30%ЃЌдђгУN2БэЪОЕФЦНОљЗДгІЫйТЪЮЊІд(N2)=___ЃЛЗДгІДяЕНЦНКтзДЬЌЪБЃЌВтЕУЖўбѕЛЏЬМЮЊ0.8molЃЌдђЦНКтЪБЕФбЙЧПЮЊЦ№ЪМбЙЧПЕФ__БЖ(БЃСєСНЮЛаЁЪ§)ЁЃ
ЂкИУЗДгІдкЕЭЮТЯТФмздЗЂНјааЃЌИУЗДгІЕФІЄH__0(ЬюЁА>ЁБЁЂЁА<ЁБ)
ЂлдкФГвЛОјШШЁЂКуШнЕФУмБеШнЦїжаГфШывЛЖЈСПЕФNOЁЂCOЗЂЩњЩЯЪіЗДгІЃЌВтЕУе§ЗДгІЕФЫйТЪЫцЪБМфБфЛЏЕФЧњЯпШчЭМЫљЪО(вбжЊЃКt2-t1=t3-t2)дђЯТСаЫЕЗЈВЛе§ШЗЕФЪЧ__(ЬюБрКХ)
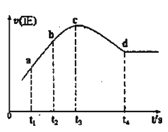
A.ЗДгІдкcЕуЮДДяЕНЦНКтзДЬЌ
B.ЗДгІЫйТЪaЕуаЁгкbЕу
C.ЗДгІЮяХЈЖШaЕуДѓгкbЕу
D.NOЕФзЊЛЏТЪЃКt1~t2 > t2~t3
ЁОД№АИЁП-312kJ/mol BC BD 0.075mol/(LЁЄmin) 0.89 ЃМ D
ЁОНтЮіЁП
ЃЈ1ЃЉвбжЊвЛЖЈЬѕМўЯТЃЌCH4КЭCH3OHЕФШМЩеШШЗжБ№784kJ/molКЭ628kJ/molЃЌМДЂйCH4(g)+ 2O2(g)=CO2(g)+2H2O(g) ЁїH1=-784kJ/molЃЌЂкCH3OH(g)+![]() O2(g)=CO2(g)+2H2O(g) ЁїH2=-628kJ/molЃЌИљОнИЧЫЙЖЈТЩЃКЂйЁС2-ЂкЁС2ПЩЕУЃЌ2CH4(g)+O2(g)=2CH3OH(g) ЁїH= -312kJ/molЃЛ
O2(g)=CO2(g)+2H2O(g) ЁїH2=-628kJ/molЃЌИљОнИЧЫЙЖЈТЩЃКЂйЁС2-ЂкЁС2ПЩЕУЃЌ2CH4(g)+O2(g)=2CH3OH(g) ЁїH= -312kJ/molЃЛ
ЃЈ2ЃЉЂйЭЈЙ§ЭМЪОПЩжЊЃЌЮТЖШдНИпЖўМзУбЕФжЪСПЗжЪ§дНаЁЃЛе§ЗДгІЮЊЦјЬхЬхЛ§МѕаЁЕФЗДгІЃЌдіДѓбЙЧПЦНКте§ЯђвЦЖЏЃЌЖўМзУбЕФжЪСПЗжЪ§діДѓЃЛ
ЂкAЃЎдіДѓЗДгІЮяХЈЖШЃЌЦНКте§ЯђвЦЖЏЃЌе§ЗДгІЫйТЪЯШдіДѓКѓМѕаЁЃЛ
BЃЎФцЗДгІЫйТЪЯШдіДѓКѓМѕаЁЃЌЫЕУїЦНКтФцЯђвЦЖЏЃЛ
CЃЎЛЏбЇЦНКтГЃЪ§KжЕдіДѓЃЌЫЕУїЦНКте§ЯђвЦЖЏЃЛ
DЃЎЗДгІЮяЕФЬхЛ§АйЗжКЌСПдіДѓЃЌЫЕУїЦНКтФцЯђвЦЖЏЃЛ
ЃЈ3ЃЉЂйИљОнCOзЊЛЏТЪМЦЫуЯћКФCOЮяжЪЕФСПЃЌИљОнv=![]() МЦЫуvЃЈCOЃЉЃЌдйИљОнЫйТЪжЎБШЕШгкЛЏбЇМЦСПЪ§жЎБШМЦЫуvЃЈN2ЃЉЃЛгЩЬтФПаХЯЂПЩжЊЃЌ
МЦЫуvЃЈCOЃЉЃЌдйИљОнЫйТЪжЎБШЕШгкЛЏбЇМЦСПЪ§жЎБШМЦЫуvЃЈN2ЃЉЃЛгЩЬтФПаХЯЂПЩжЊЃЌ
РћгУШ§ЖЮЪНЃК2NO(g)+2CO(g)![]() 2CO2(g) +N2(g)
2CO2(g) +N2(g)
Ц№ЪМ(mol) 1.5mol 2.0mol 0 0
БфЛЏ(mol) 0.8mol 0.8mol 0.8mol 0.4mol
ЦНКт(mol) 0.7mol 1.2mol 0.8mol 0.4mol
ИљОнЮяжЪЕФСПжЎБШ=бЙЧПжЎБШПЩЕУЃЌЦНКтЪБЕФбЙЧПЃКЦ№ЪМбЙЧП=ЦНКтЪБЕФЮяжЪЕФСПЃКГѕЪМЮяжЪЕФСПЃЛ
Ђке§ЗДгІЮЊЦјЬхЮяжЪЕФСПМѕаЁЕФЗДгІЃЌЮЊьиМѕЗДгІЃЌЖјЁїH-TЁїS<0ЗДгІздЗЂНјааЃЛ
ЂлДгt4ЪБПЬе§ЗДгІЫйТЪВЛБфЃЌДІгкЦНКтзДЬЌЃЌt4ЪБПЬЧАЮДЕНДяЦНКтЃЌЗДгІЯђе§ЗДгІНјааЃЌгЩЂкжаПЩжЊЮЊЗДгІШШЗДгІЃЌОјШШЬѕМўЯТЃЌЫцЗДгІНјааЮТЖШЩ§ИпЃЌЮТЖШЦ№жїЕМзїгУЃЌЗДгІЫйТЪМгПьЃЌЖјКѓХЈЖШЮЊжїЕМвђЫиЃЌЗДгІЫйТЪМѕЕЭжСЦНКтзДЬЌЃЛ
ЃЈ1ЃЉвбжЊвЛЖЈЬѕМўЯТЃЌCH4КЭCH3OHЕФШМЩеШШЗжБ№784kJ/molКЭ628kJ/molЃЌМДЂйCH4(g)+ 2O2(g)=CO2(g)+2H2O(g) ЁїH1=-784kJ/molЃЌЂкCH3OH(g)+![]() O2(g)=CO2(g)+2H2O(g) ЁїH2=-628kJ/molЃЌИљОнИЧЫЙЖЈТЩЃКЂйЁС2-ЂкЁС2ПЩЕУЃЌ2CH4(g)+O2(g)=2CH3OH(g) ЁїH= -312kJ/molЃЌ
O2(g)=CO2(g)+2H2O(g) ЁїH2=-628kJ/molЃЌИљОнИЧЫЙЖЈТЩЃКЂйЁС2-ЂкЁС2ПЩЕУЃЌ2CH4(g)+O2(g)=2CH3OH(g) ЁїH= -312kJ/molЃЌ
ЙЪД№АИЮЊЃК-312kJ/molЃЛ
ЃЈ2ЃЉЂй2CO(g)+4H2(g) CH3OCH3(g) +H2O(g) ЁїH<0ЃЌе§ЗДгІЗХШШЃЌгЩЭМЪОПЩжЊЮТЖШдНИпЖўМзУбЕФжЪСПЗжЪ§дНаЁЃЌЙЪЮТЖШЃКT1>T2>T3>T4ЃЛе§ЗДгІЮЊЦјЬхЬхЛ§МѕаЁЕФЗДгІЃЌдіДѓбЙЧПЦНКте§ЯђвЦЖЏЃЌЖўМзУбЕФжЪСПЗжЪ§діДѓЃЌЙЪбЙЧПP1>P2>P3>P4ЃЌ
ЙЪД№АИЮЊЃКBCЃЛ
ЂкAЃЎдіДѓЗДгІЮяХЈЖШЃЌЦНКте§ЯђвЦЖЏЃЌе§ЗДгІЫйТЪЯШдіДѓКѓМѕаЁЃЌВЛвЛЖЈФцЯђвЦЖЏЃЌЙЪAДэЮѓЃЛ
BЃЎФцЗДгІЫйТЪЯШдіДѓКѓМѕаЁЃЌЫЕУїЦНКтФцЯђвЦЖЏЃЌЙЪBе§ШЗЃЛ
CЃЎЛЏбЇЦНКтГЃЪ§KжЕдіДѓЃЌЫЕУїЦНКте§ЯђвЦЖЏЃЌЙЪCДэЮѓЃЛ
DЃЎЗДгІЮяЕФЬхЛ§АйЗжКЌСПдіДѓЃЌЫЕУїЦНКтФцЯђвЦЖЏЃЌЙЪDе§ШЗЃЛ
ЙЪД№АИбЁBDЃЛ
ЃЈ3ЃЉЂйЯћКФCOЮяжЪЕФСПЮЊ2.0molЁС30%=0.6molЃЌv(CO)= =0.15mol/(LЁЄmin)ЃЌЫйТЪжЎБШЕШгкЛЏбЇМЦСПЪ§жЎБШЃЌдђv(N2)=
=0.15mol/(LЁЄmin)ЃЌЫйТЪжЎБШЕШгкЛЏбЇМЦСПЪ§жЎБШЃЌдђv(N2)=![]() v(CO)=
v(CO)=![]() ЁС0.15mol/(LЁЄmin)=0.075 mol/(LЁЄmin)ЃЛ
ЁС0.15mol/(LЁЄmin)=0.075 mol/(LЁЄmin)ЃЛ
РћгУШ§ЖЮЪНЃК2NO(g)+2CO(g)![]() 2CO2(g) +N2(g)
2CO2(g) +N2(g)
Ц№ЪМ(mol) 1.5mol 2.0mol 0 0
БфЛЏ(mol) 0.8mol 0.8mol 0.8mol 0.4mol
ЦНКт(mol) 0.7mol 1.2mol 0.8mol 0.4mol
ИљОнЮяжЪЕФСПжЎБШ=бЙЧПжЎБШПЩЕУЃЌЦНКтЪБЕФбЙЧПЃКЦ№ЪМбЙЧП=ЦНКтЪБЕФЮяжЪЕФСПЃКГѕЪМЮяжЪЕФСП=![]() = 0.89ЃЌдђЦНКтЪБЕФбЙЧПЮЊЦ№ЪМбЙЧПЕФ0.89БЖЃЌ
= 0.89ЃЌдђЦНКтЪБЕФбЙЧПЮЊЦ№ЪМбЙЧПЕФ0.89БЖЃЌ
ЙЪД№АИЮЊЃК0.075 mol/(LЁЄmin)ЃЛ0.89ЃЛ
Ђке§ЗДгІЮЊЦјЬхЮяжЪЕФСПМѕаЁЕФЗДгІЃЌЮЊьиМѕЗДгІЃЌЁїS<0ЃЌЖјЁїH-TЁїS<0ЗДгІздЗЂНјааЃЌИУЗДгІдкЕЭЮТЯТФмздЗЂНјааЃЌИУЗДгІЕФЁїH<0ЃЌ
ЙЪД№АИЮЊЃК<ЃЛ
ЂлДгt4ЪБПЬе§ЗДгІЫйТЪВЛБфЃЌДІгкЦНКтзДЬЌЃЌt4ЪБПЬЧАЮДЕНДяЦНКтЃЌЗДгІЯђе§ЗДгІНјааЃЌгЩЂкжаПЩжЊЮЊЗДгІШШЗДгІЃЌОјШШЬѕМўЯТЃЌЫцЗДгІНјааЮТЖШЩ§ИпЃЌЮТЖШЦ№жїЕМзїгУЃЌЗДгІЫйТЪМгПьЃЌЖјКѓХЈЖШЮЊжїЕМвђЫиЃЌЗДгІЫйТЪМѕЕЭжСЦНКтзДЬЌЃЛ
AЃЎЗДгІдкcЕуЮДДяЕНЦНКтзДЬЌЃЌЙЪAе§ШЗЃЛ
BЃЎгЩЭМПЩжЊЃЌЗДгІЫйТЪaЕуаЁгкbЕуЃЌЙЪBе§ШЗЃЛ
CЃЎЗДгІЮяХЈЖШaЕуДѓгкbЕуЃЌЙЪCе§ШЗЃЛ
DЃЎNOЕФзЊЛЏТЪЃКt1ЁЋt2<t2ЁЋt3ЃЌЙЪDДэЮѓЃЌ
ЙЪД№АИбЁDЁЃ

ЁОЬтФПЁПвбжЊЗДгІX(g)ЃЋY(g)![]() R(g)ЃЋQ(g)ЕФЦНКтГЃЪ§гыЮТЖШЕФЙиЯЕШчБэЫљЪОЁЃ830 ЁцЪБЃЌЯђвЛИі2 LЕФУмБеШнЦїжаГфШы0.2 mol XКЭ0.8 mol YЃЌЗДгІГѕЪМ4 sФкv(X)ЃН0.005 mol/(LЁЄs)ЁЃЯТСаЫЕЗЈе§ШЗЕФЪЧ
R(g)ЃЋQ(g)ЕФЦНКтГЃЪ§гыЮТЖШЕФЙиЯЕШчБэЫљЪОЁЃ830 ЁцЪБЃЌЯђвЛИі2 LЕФУмБеШнЦїжаГфШы0.2 mol XКЭ0.8 mol YЃЌЗДгІГѕЪМ4 sФкv(X)ЃН0.005 mol/(LЁЄs)ЁЃЯТСаЫЕЗЈе§ШЗЕФЪЧ
ЮТЖШ/Ёц | 700 | 800 | 830 | 1 000 | 1 200 |
ЦНКтГЃЪ§ | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
A. 4 sЪБШнЦїФкc(Y)ЃН0.76 mol/L
B. 830 ЁцДяЦНКтЪБЃЌXЕФзЊЛЏТЪЮЊ80%
C. ЗДгІДяЦНКтКѓЃЌЩ§ИпЮТЖШЃЌЦНКте§ЯђвЦЖЏ
D. 1 200 ЁцЪБЗДгІR(g)ЃЋQ(g) ![]() X(g)ЃЋY(g)ЕФЦНКтГЃЪ§KЃН0.4
X(g)ЃЋY(g)ЕФЦНКтГЃЪ§KЃН0.4