题目内容
【题目】半导体光催化CO2机理如图甲所示,设计成电化学装置如图乙所示,则下列说法正确的是( )
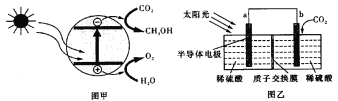
A.若导线上有4mol电子移动,则质子交换膜左侧产生22.4 L O2
B.装置中进行的总反应一定是自发的氧化还原反应
C.b极上的电极反应为:CO2+6H+-6e-=CH3OH+H2O
D.图乙中的能量转化形式为:光能→电能→化学能
【答案】D
【解析】
A.未指明温度和压强无法确定气体的体积,故A错误;
B.该装置有外界条件:光照,所以装置中进行的不一定是自发进行的氧化还原反应,故B错误;
C.根据图甲可知通入的二氧化碳转化为甲醇,得电子发生发生还原反应,电极方程式为CO2+6H++6e-=CH3OH+H2O,故C错误;
D.通过半导体将光能转化为电能,再通过电解质将电能转化为化学能,故D正确;
故答案为D。

 智能训练练测考系列答案
智能训练练测考系列答案【题目】在相同的密闭容器中,用高纯度纳米级Cu2O分别进行催化分解水的实验:2 H2O(g)![]() 2 H2(g) + O2(g) H>0,实验测得反应体系中水蒸气浓度(mol·L-1)的变化结果如下:
2 H2(g) + O2(g) H>0,实验测得反应体系中水蒸气浓度(mol·L-1)的变化结果如下:
序号 | 时间/min | 0 | 10 | 20 | 30 | 40 | 60 |
① | 温度T1 / 1号Cu2O | 0.0500 | 0.0492 | 0.0486 | 0.0482 | 0.0480 | 0.0480 |
② | 温度T1 / 2号Cu2O | 0.0500 | 0.0490 | 0.0483 | 0.0480 | 0.0480 | 0.0480 |
③ | 温度T2 / 2号Cu2O | 0.0500 | 0.0480 | 0.0470 | 0.0470 | 0.0470 | 0.0470 |
下列说法不正确的是( )
A. 实验时的温度T2高于T1
B. 2号Cu2O的催化效率比1号Cu2O的催化效率高
C. 实验①前20 min的平均反应速率v(O2) = 7×10ˉ5 mol·Lˉ1·minˉ1
D. 等质量纳米级Cu2O比微米级Cu2O催化效率高,这与Cu2O的粒径大小有关
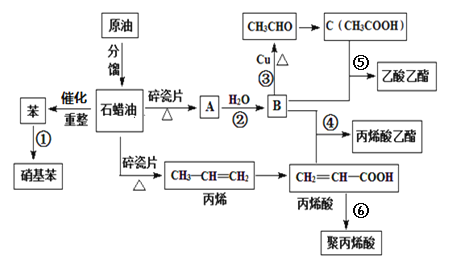
【题目】有机物R是合成某药物的中间体,结构简式为![]() 。下列说法正确的是
。下列说法正确的是
A.R与M( )互为同分异构体B.R中所有碳原子一定处于同一平面
)互为同分异构体B.R中所有碳原子一定处于同一平面
C.R的六元环上的一氯代物有4种D.R能发生取代反应、加成反应和氧化反应
【题目】下列有关实验的仪器选择和部分实验操作均正确的是( )
选项 | 实验 | 所选主要仪器铁架台等忽略 | 部分操作 |
A | 用浓硫酸配制480mL0.1mol/L硫酸溶液 | 500mL容量瓶、烧杯、玻璃棒、量筒、胶头滴管 | 将刚稀释所得的硫酸溶液立刻转移至500mL容量瓶,并加水至刻度线即可 |
B | 从食盐水中得到NaCl晶体 | 坩埚、酒精灯、玻璃棒、泥三角、三脚架 | 当加热至大量晶体出现时,停止加热,利用余热继续蒸干 |
C | 从碘的四氯化碳溶液中得到碘 | 蒸馏烧瓶、酒精灯、温度计、冷凝管、锥形瓶、牛角管 | 温度计水银球插入液液面以下 |
D | 用汽油提取溴水中的Br2 | 分液漏斗、烧杯 | 分离时下层液体从分液漏斗下口放出,上层液体从上口倒出 |
A.AB.BC.CD.D