题目内容
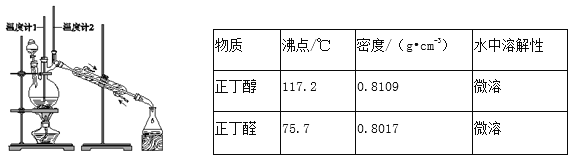
【题目】化学上常用燃烧法确定有机物的组成。这种方法是在电炉加热时用纯氧气氧化管内样品,根据产物的质量确定有机物的组成。下列装置是用燃烧法确定有机物分子式常用的装置。
回答下列问题:
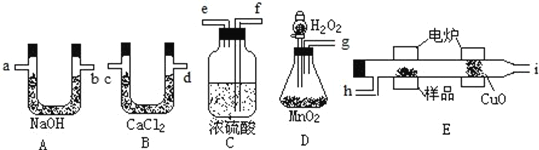
(1)产生的氧气按从左到右流向,所选装置的连接顺序为_________________;
(2)C装置中浓硫酸的作用是__________________;
(3)D装置中MnO2的作用是___________________;
(4)燃烧管中CuO的作用是________________;
(5)若准确称取0.90g样品CxHyOz,经充分燃烧后,A管质量增加1.32g,B管质量增加0.54g,则x:y:z为________________。
【答案】 g﹣f﹣e﹣h﹣i﹣c﹣d﹣a﹣b 干燥氧气 催化剂 防止生成CO 1:2:1
【解析】分析:利用双氧水分解生成氧气,由于生成的氧气中含有水蒸气,与样品反应前需要首先净化,利用浓硫酸除去水蒸气。有机物燃烧产生水蒸气和二氧化碳,利用无水氯化钙吸水,氢氧化钠吸收二氧化碳,根据水蒸气和二氧化硫的质量结合质量守恒定律计算有机物的最简式。
详解:(1)D中生成的氧气中含有水蒸气,应先通过C中的浓硫酸干燥,在E中电炉加热时用纯氧氧化管内样品,生成二氧化碳和水,如有一氧化碳生成,则E中CuO可与CO进一步反应生成二氧化碳,然后分别通入B(吸收水)、A(吸收二氧化碳)中,根据产物的质量推断有机物的组成,则产生的氧气按从左到右流向,所选择装置各导管的连接顺序是g-f-e-h-i-c-d-a-b;
(2)D中生成的氧气中含有水蒸气,应先通过C中的浓硫酸干燥,以免影响实验结果,所以浓硫酸的作用是干燥氧气;
(3)MnO2为分解双氧水制备氧气的催化剂;
(4)一氧化碳能与氧化铜在加热时发生反应,产生Cu与CO2,因此CuO的作用是把有机物不完全燃烧产生的CO转化为CO2,防止生成CO;
(5)A管质量增加1.32g说明生成了1.32g二氧化碳,物质的量是1.32g÷44g/mol=0.03mol,可得碳元素的质量:m(C)=0.03mol×12g/mol=0.36g;B管质量增加0.54g说明生成了0.54g水,物质的量是0.54g÷18g/mol=0.03mol,可得氢元素的质量:m(H)=0.06g,根据质量守恒定律可知含氧元素的质量为m(O)=0.90g-0.36g-0.06g=0.48g,n(O)=0.48g÷16g/mol=0.03mol,所以n(C):n(H):n(O)=1:2:1,所以x:y:z=1:2:1。