题目内容
【题目】下列事实不能用勒夏特列原理解释的是
A. 开启啤酒瓶后,瓶中马上泛起大量泡沫
B. H2、I2、HI混合气体加压后颜色变深
C. 红棕色的NO2加压后颜色先变深再变浅
D. 工业上生产硫酸的过程中使用过量的空气,以提高二氧化硫的利用率
【答案】B
【解析】
如果改变影响平衡的1个条件,平衡就向能够减弱这种改变的方向进行,中这就是勒夏特列原理,该原理适用于所有的平衡体系。
A、开启啤酒瓶后,越强减小,气体的溶解度减小,因此瓶中马上泛起大量泡沫,A可以用勒夏特列原理解释;
B、反应H2+I2![]() 2HI是体积不变的可逆反应,因此H2、I2、HI混合气体加压后平衡不移动,但单质碘的浓度增大,因此颜色变深,B不能用勒夏特列原理解释;
2HI是体积不变的可逆反应,因此H2、I2、HI混合气体加压后平衡不移动,但单质碘的浓度增大,因此颜色变深,B不能用勒夏特列原理解释;
C、NO2存在平衡关系2NO2![]() N2O4,因此红棕色的NO2加压后平衡向正反应方向移动,所以颜色先变深再变浅,C可以用勒夏特列原理解释;
N2O4,因此红棕色的NO2加压后平衡向正反应方向移动,所以颜色先变深再变浅,C可以用勒夏特列原理解释;
D、SO2与氧气反应的方程式为2SO2+O2![]() 2SO3,增大氧气的浓度平衡向正反应方向移动,因此SO2的转化率增大,D可以用勒夏特列原理解释.
2SO3,增大氧气的浓度平衡向正反应方向移动,因此SO2的转化率增大,D可以用勒夏特列原理解释.
答案选B。

 阅读快车系列答案
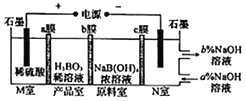
阅读快车系列答案【题目】中和热的测定是高中化学中重要的定量实验。取50mL、0.55mol/L的NaOH溶液与50mL、0.25mol/L的H2SO4溶液置于如图所示的装置中进行中和热的测定实验,回答下列问题:
(1)从如图所示实验装置看,其中尚缺少的一种玻璃用品是_____________,除此之外,装置的一个明显错误是___________________________________________________。

(2)NaOH溶液稍过量的原因是_______________________________________________。
(3)若改用60mL、0.25mol/L的H2SO4溶液和50mL、0.55mol/L的NaOH溶液进行反应,与上述实验相比,所放出的热量_____________(填“相等”或“不相等”),若实验操作均正确,则所求中和热_______________(填“相等”或“不相等”)。
(4)倒入NaOH溶液的正确操作是__________
A.沿玻璃棒缓慢倒入 B.分三次少量倒入 C.一次性迅速倒入
(5)实验数据如下表:
温度 实验次数 | 起始温度t1/℃ | 终止温度t2/℃ | 温度差平均值 (t2-t1)/℃ | ||
H2SO4 | NaOH | 平均值 | |||
1 | 26.2 | 26.0 | 26.1 | 29.5 | |
2 | 27.0 | 27.4 | 27.2 | 32.3 | |
3 | 25.9 | 25.9 | 25.9 | 29.2 | |
4 | 26.4 | 26.2 | 26.3 | 29.8 | |
①近似认为0.55mol/L NaOH溶液和0.25mol/L H2SO4溶液的密度都是1g/cm3,中和后生成溶液的比热容c=4.18J/(g℃),则中和热△H=__________(取小数点后一位)。
②上述实验的结果与57.3kJ/mol有偏差,产生偏差的原因可能是____________。
A.实验装置保温、隔热效果差
B.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
C.做实验的当天室温较高
D.量取H2SO4时仰视读数