题目内容
下列实验中操作、现象、结论对应关系正确的一组是( )
| 选项 | 操作 | 现象 | 结论 |
| A | 在蔗糖中加入几滴水搅拌均匀,再加入浓硫酸,迅速搅拌 | 蔗糖逐渐变黑,体积膨胀,形成疏松多孔的物质 | 体现了浓硫酸的脱水性、氧化性及酸性 |
| B | 淀粉和稀硫酸混合共热后,再加少量新制氢氧化铜悬浊液 | 产生红色沉淀 | 淀粉水解可生成葡萄糖 |
| C | 硫酸铵溶液滴入蛋白质溶液中 | 生成白色沉淀 | 蛋白质溶液发生了盐析 |
| D | 苯滴入溴水中并充分振荡,并静置 | 溴水不褪色 | 苯与溴水不发生化学反应 |
| A、A | B、B | C、C | D、D |
考点:化学实验方案的评价
专题:实验评价题
分析:A.没有盐类物质生成,浓硫酸不表现酸性;
B.酸性条件下不可能生成红色沉淀;
C.蛋白质在硫酸铵溶液中发生盐析;
D.溴易溶于苯.
B.酸性条件下不可能生成红色沉淀;
C.蛋白质在硫酸铵溶液中发生盐析;
D.溴易溶于苯.
解答:
解:A.浓硫酸可使蔗糖脱水而碳化,碳和浓硫酸反应生成二氧化碳和二氧化硫,没有盐类物质生成,浓硫酸不表现酸性,故A错误;
B.酸性条件下不可能生成红色沉淀,在酸性条件下水解后应先加入碱使溶液至碱性,然后在加入氢氧化铜浊液在加热条件下反应,故B错误;
C.蛋白质在硫酸铵溶液中发生盐析,故C正确;
D.溴易溶于苯,溴水褪色,但没有发生化学反应,为萃取过程,故D错误.
故选C.
B.酸性条件下不可能生成红色沉淀,在酸性条件下水解后应先加入碱使溶液至碱性,然后在加入氢氧化铜浊液在加热条件下反应,故B错误;
C.蛋白质在硫酸铵溶液中发生盐析,故C正确;
D.溴易溶于苯,溴水褪色,但没有发生化学反应,为萃取过程,故D错误.
故选C.
点评:本题综合考查化学实验方案的评价,涉及物质的性质、检验以及分离等知识,侧重于学生的分析能力和实验能力的考查,为高考常见题型,注意把握实验的严密性和可行性的评价,难度中等.

练习册系列答案
 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案
相关题目
固体NH5属于离子晶体.它与水反应的化学方程式为NH5+H2O→NH3?H2O+H2↑,它也能跟乙醇发生类似的反应,并都产生氢气.下列有关NH5叙述正确的是( )
| A、含有NH4+和H- |
| B、NH5中N元素的化合价为+5价 |
| C、1mol NH5中含有5NA个N-H键 |
| D、与乙醇反应时,NH5被还原 |
下列反应中,属于加成反应的是( )
| A、甲烷与氯气反应制取一氯甲烷 |
| B、乙酸与乙醇反应制取乙酸乙酯 |
| C、苯酚与饱和溴水反应生成三溴苯酚 |
| D、乙烯与氯化氢反应制取氯乙烷 |
25℃、101kPa下:①2Na(s)+
O2(g)═Na2O(s)△H1=-414kJ?mol-1②2Na(s)+O2(g)═Na2O2(s)△H2=-511kJ?mol-1,下列说法正确的是( )
| 1 |
| 2 |
| A、①和②产物的阴阳离子个数比不相等 |
| B、①和②生成等物质的量的产物,转移电子数不同 |
| C、25℃、101kPa下,Na2O2(s)+2Na(s)═2Na2O(s)△H=-317 kJ?mol-1 |
| D、常温下Na与足量O2反应生成Na2O,随温度升高生成Na2O的速率逐渐加快 |
下列各组金属最适合用H2或CO把它从化合物中还原出来的为( )
| A、Ca Mg |
| B、Al Fe |
| C、Fe Cu |
| D、Hg Ag |
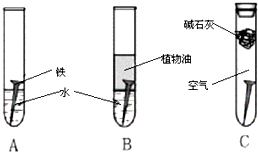 某研究小组对铁生锈进行研究:
某研究小组对铁生锈进行研究: