题目内容
16.下列有关除杂的实验操作合理的是( )| A. | 除去二氧化碳中混有的少量一氧化碳:通入适量氧气后点燃 | |
| B. | 除去硝酸钾晶体里少量的氯化钠:加水溶解,蒸发结晶至有大量晶体析出,停止加热用余热蒸干 | |
| C. | 除去氮气中少量氧气:使气体通过炽热的铜粉 | |
| D. | 除去氯化钠固体中少量的纯碱:加入足量氯化钙,过滤、蒸发、结晶 |
分析 A.在二氧化碳中CO不易点燃,且引入新杂质氧气;
B.硝酸钾、氯化钠均溶于水,但二者溶解度受温度影响不同;
C.氧气与Cu反应,而氮气不能;
D.纯碱与氯化钙反应生成沉淀和氯化钠,但氯化钙足量引入新杂质.
解答 解:A.在二氧化碳中CO不易点燃,且引入新杂质氧气,不能除杂,应通过灼热的CuO,故A错误;
B.硝酸钾、氯化钠均溶于水,但二者溶解度受温度影响不同,应利用冷却结晶分离,不能蒸发结晶,故B错误;
C.氧气与Cu反应,而氮气不能,气体通过炽热的铜粉可除杂,故C正确;
D.纯碱与氯化钙反应生成沉淀和氯化钠,但氯化钙足量引入新杂质,应加适量的氯化钙,故D错误;
故选C.
点评 本题考查化学实验方案的评价,为高频考点,涉及混合物分离提纯、物质的性质等,把握反应原理和除杂的原则为解答的关键,侧重分析与实验能力的考查,题目难度不大.

练习册系列答案
 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案 双基同步导航训练系列答案
双基同步导航训练系列答案
相关题目
7.下列设计的实验方案能达到实验目的是( )
| A. | 通过灼热的镁粉除去N2中的O2 | |
| B. | 用湿润碘化钾淀粉试纸鉴别Br2(g)和NO2 | |
| C. | 向沸水中滴加饱和FeCl3溶液制备Fe(OH)3胶体 | |
| D. | 检验溶液中是否有SO42-:先将溶液用足量的盐酸酸化,再加入BaCl2溶液 |
11.在①硫酸 ②芒硝(Na2SO4•10H2O) ③三氧化硫 ④硫酸亚铁四种化合物中,硫元素的质量分数由高到低的顺序是( )
| A. | ①>②>③>④ | B. | ③>①>④>② | C. | ①>③>④>② | D. | ②>③>④>① |

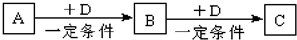 已知A、B、C是中学化学的常见物质,它们在一定条件下有如图转化关系:
已知A、B、C是中学化学的常见物质,它们在一定条件下有如图转化关系: