题目内容

C
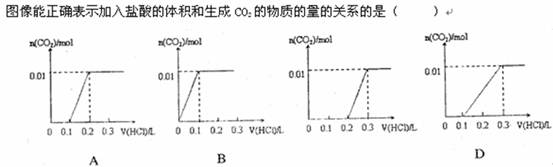
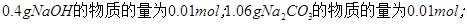 当向溶液中滴加0.1mol/L的稀盐酸时,稀盐酸先与NaOH反应,需消耗稀盐酸体积为100Ml;反应完全后,稀盐酸再与碳酸钠溶液反应,先生成碳酸氢钠,需消耗稀盐酸的体积为100Ml;再生成二氧化碳和水,需消耗稀盐酸的体积为100Ml;
当向溶液中滴加0.1mol/L的稀盐酸时,稀盐酸先与NaOH反应,需消耗稀盐酸体积为100Ml;反应完全后,稀盐酸再与碳酸钠溶液反应,先生成碳酸氢钠,需消耗稀盐酸的体积为100Ml;再生成二氧化碳和水,需消耗稀盐酸的体积为100Ml;所以正确选项为C;

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
题目内容


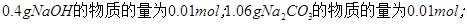 当向溶液中滴加0.1mol/L的稀盐酸时,稀盐酸先与NaOH反应,需消耗稀盐酸体积为100Ml;反应完全后,稀盐酸再与碳酸钠溶液反应,先生成碳酸氢钠,需消耗稀盐酸的体积为100Ml;再生成二氧化碳和水,需消耗稀盐酸的体积为100Ml;
当向溶液中滴加0.1mol/L的稀盐酸时,稀盐酸先与NaOH反应,需消耗稀盐酸体积为100Ml;反应完全后,稀盐酸再与碳酸钠溶液反应,先生成碳酸氢钠,需消耗稀盐酸的体积为100Ml;再生成二氧化碳和水,需消耗稀盐酸的体积为100Ml;
 阅读快车系列答案
阅读快车系列答案