��Ŀ����
����Ŀ����1������֪��ԭ�ӽṹ���ɣ�27��Ԫ�������ڱ��е�λ����____________����۵��ӵĹ���Ų�ͼΪ_____________________________��
��2����en�����Ҷ���(![]() ),�������[Pt(en)2]Cl4�������ӵ���λԭ����Ϊ____________��
),�������[Pt(en)2]Cl4�������ӵ���λԭ����Ϊ____________��
��3��BeCl2�ǹ��۷��ӣ������Ե��塢������Ͷ������ʽ���ڡ����ǵĽṹ��ʽ���£�ָ��Be���ӻ�������͡�
��Cl-Be-Cl ____________��
�� ![]() ____________��
____________��
��![]() ___________��
___________��
��4������(BP)��һ���м�ֵ����ĥӲͿ����ϣ������մɲ��Ͽ���Ϊ��������ı�����Ĥ������ͨ���ڸ���������Χ��(>750��)���廯������廯��Ӧ�Ƶá�BP������ͼ��ʾ��
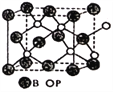
�ٻ������廯������廯�Ŀռ�ṹʽ(�������ֳ���������ṹ)��
���廯��____________________��
���廯��____________________��
����BP������B�Ķѻ���ʽΪ____________��
�ۼ��㵱��������Ϊ478pm(��ͼ���������ÿ���߳�Ϊ478pm)ʱ��������ԭ�Ӻ���ԭ��֮����������____________��
���𰸡� �������ڢ��� ![]() 4 sp sp2 sp3
4 sp sp2 sp3 ![]()
![]() �����������ܶѻ� 207pm��239
�����������ܶѻ� 207pm��239![]() /2
/2
�������������������1��27��Ԫ��ԭ��3d����Ų�7�����ӣ�λ��Ԫ�����ڱ��е�������VIII�壻3d74s2Ϊ�۵��ӣ�����Ų�ͼΪ��![]() ��
��
��2���Ҷ�������2��Nԭ��������ԭ����λ�����������[Pt��en��2]Cl4�������ӵ���λԭ����Ϊ4��
��3��������![]() ��֪Be�γ��������ӻ����������Be���ӻ��������Ϊsp��
��֪Be�γ��������ӻ����������Be���ӻ��������Ϊsp��
������![]() ��֪Be�γ���3���ӻ����������Be���ӻ��������Ϊsp2��
��֪Be�γ���3���ӻ����������Be���ӻ��������Ϊsp2��
������![]() ��֪Be�γ���4���ӻ����������Be���ӻ��������Ϊsp3��
��֪Be�γ���4���ӻ����������Be���ӻ��������Ϊsp3��
��4����Bԭ�Ӻ���3���۵��ӣ���3��Brԭ���γ��������ռ乹��Ϊƽ�������Σ��������廯��Ŀռ�ṹʽΪ��![]() ��Pԭ�Ӻ���5���۵��ӣ���3��Brԭ���γ�����������1�Ե��Ӷԣ��ռ乹��Ϊ�����Σ��������廯�Ŀռ�ṹʽΪ��
��Pԭ�Ӻ���5���۵��ӣ���3��Brԭ���γ�����������1�Ե��Ӷԣ��ռ乹��Ϊ�����Σ��������廯�Ŀռ�ṹʽΪ��![]() ��
��
������BP�ľ���ʾ��ͼ��֪B�Ķѻ���ʽΪ���������ѻ���
������BP�ľ���ʾ��ͼ��֪��ԭ�Ӻ���ԭ��֮������������ھ�����Խ��ߵ�1/4�����������Ϊx����4x=![]() 478�����x=207pm��239
478�����x=207pm��239![]() /2 pm��
/2 pm��

 ������Ӧ���ϵ�д�
������Ӧ���ϵ�д� ��ʦ�㾦�ִʾ��ƪϵ�д�
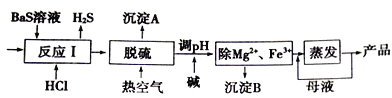
��ʦ�㾦�ִʾ��ƪϵ�д�����Ŀ��������һ�����͵���ɫ��Դ������һ����Ҫ�Ļ���ԭ�ϡ���������ʣ���C �ƣ���ˮ������Ӧ��ȡH2��һ�ֵͺ��ܣ���Ч�ʵ���H2�������÷���������¯����H2��ȼ��¯����CaO�������ɡ�����¯���漰���ķ�ӦΪ��
I.C��s��+H2O��g��![]() CO��g��+H2��g�� K1��
CO��g��+H2��g�� K1��
��.CO��g��+H2O��g��![]() CO2��g��+H2��g�� K2��
CO2��g��+H2��g�� K2��
��.CaO��s��+CO2��g��![]() CaCO3��s�� K3��
CaCO3��s�� K3��
��1���ù�����H2�ܷ�Ӧ�ɱ�ʾΪC(s)+2H2O(g)+CaO(s)![]() CaCO3(s)+2H2(g)���䷴Ӧ��ƽ�ⳣ��K=_______________����K1��K2��K3�Ĵ���ʽ��ʾ������2L���ܱ������м���һ������C(s)��H2O(g)��CaO(s)��������˵����Ӧ�ﵽƽ��״̬����__________��
CaCO3(s)+2H2(g)���䷴Ӧ��ƽ�ⳣ��K=_______________����K1��K2��K3�Ĵ���ʽ��ʾ������2L���ܱ������м���һ������C(s)��H2O(g)��CaO(s)��������˵����Ӧ�ﵽƽ��״̬����__________��
a�������ڻ������������� b��H2��H2O��g�������ʵ���֮�Ȳ��ٱ仯
c�����������ܶȲ��ٱ仯 d���γ� a mol H-H����ͬʱ���� 2 amol H-O��
��2�����ڷ�Ӧ������ͬ�¶Ⱥ�ѹǿ��H2����Ӱ�����±���
ѹǿ �¶� | p1/Mpa | p2/Mpa |
500�� | 45.6% | 51.3% |
700�� | 67.8% | 71.6% |
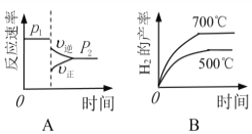
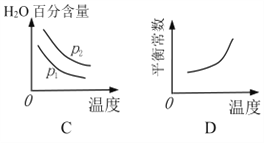
�ɱ��������жϣ�p1 ______ p2���������������������
����ͼ����ȷ����_________��
��3����֪��Ӧ������H= ��41.1 kJ/mol�� C��O��O��H��H��H�ļ��ֱܷ�Ϊ803kJ/mol��464 kJ/mol��436 kJ/mol���� CO��̼�����ļ���Ϊ___________ kJ/mol��
��4�����ڷ�Ӧ������ƽ��ʱ�ٳ���CO2��ʹ��Ũ������ԭ����2������ƽ����_____________����������Ӧ�������淴Ӧ���������ƶ���������ƽ���CO2Ũ��_________�����������������С����������������
����Ŀ��ʵ�����Ա���ȩΪԭ���Ʊ����屽��ȩ��ʵ��װ�ü�ͼ��������ʵķе����������
������������ʵķе㣨101KPa��
���� | �е�/�� | ���� | �е�/�� |
�� | 58.8 | 1��2���������� | 83.5 |
����ȩ | 179 | ���屽��ȩ | 229 |
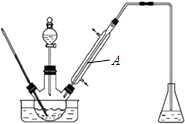
��ʵ�鲽��Ϊ��
����1��������ƿ�е�һ����ȵ���ˮAlCl3��1��2����������ͱ���ȩ��ֻ�Ϻ�������60�棬�����μӾ�H2SO4�������Һ�壬���·�Ӧһ��ʱ�䣬��ȴ��
����2������Ӧ����ﻺ������һ������ϡ�����У����衢���á���Һ���л�����10%NaHCO3��Һϴ�ӣ�
����3����ϴ�ӵ��л������������ˮMgSO4���壬����һ��ʱ�����ˣ�
����4����ѹ�����л��࣬�ռ���Ӧ��֣�
��1��ʵ��װ��A�������� �� ��ƿ�е���ҺӦΪ ��
��2������1������������У���һ�������Ǵ������仯ѧʽΪ��
��3������2����10%NaHCO3��Һϴ���л��࣬��Ϊ�˳�ȥ�����л�������ѧʽ����
��4������3�м�����ˮMgSO4����������� �� ����ķ�������
��5������4�в��ü�ѹ����������Ϊ�˷�ֹ ��