题目内容
【题目】某有机物的结构简式为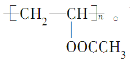 下列叙述正确的是
下列叙述正确的是
A. 1 mol该有机物与NaOH溶液完全反应时,消耗1 mol NaOH
B. 该有机物可通过加聚反应生成
C. 该有机物水解所得的产物能发生加成反应
D. 该有机物分子的单体为两种
【答案】B
【解析】
从结构上看,合成该有机物的反应为:n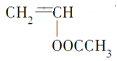
![]()
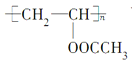 ,为加聚反应。
,为加聚反应。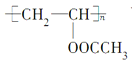 为酯类,既能在酸性条件下水解,也能在碱性条件下水解。由于1mol该有机物中含n mol酯基,因此水解时所需的水为n mol,生成了n mol乙酸和1mol
为酯类,既能在酸性条件下水解,也能在碱性条件下水解。由于1mol该有机物中含n mol酯基,因此水解时所需的水为n mol,生成了n mol乙酸和1mol 。据此解题。
。据此解题。
A. 从结构上看,该有机物为高分子,1 mol该有机物与NaOH溶液完全反应时,将消耗n mol NaOH,A项错误;
B. 合成该有机物的反应为:n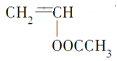
![]()
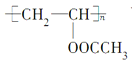 ,为加聚反应,B项正确;
,为加聚反应,B项正确;
C. 该有机物发生的水解反应为: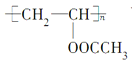 +H2O
+H2O![]()
 +n
+n![]() 所得的产物不含碳碳双键等可以发生加成反应的官能团,因此无法发生加成反应,C项错误;
所得的产物不含碳碳双键等可以发生加成反应的官能团,因此无法发生加成反应,C项错误;
D. 从合成该有机物的反应为:n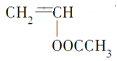
![]()
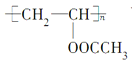 来看,合成该有机物分子的单体为
来看,合成该有机物分子的单体为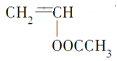 ,D项错误;
,D项错误;
答案应选B。

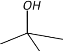
【题目】下面是丁醇的两种同分异构体,其结构简式、沸点及熔点如下表所示:
异丁醇 | 叔丁醇 | |
结构简式 |
|
|
沸点/℃ | 108 | 82.3 |
熔点/℃ | -108 | 25.5 |
下列说法不正确的是
A. 用系统命名法给异丁醇命名为:2-甲基-1-丙醇
B. 异丁醇的核磁共振氢谱有三组峰,且面积之比是1∶2∶6
C. 用降温结晶的方法可将叔丁醇从二者的混合物中结晶出来
D. 两种醇发生消去反应后得到同一种烯烃
【题目】NaNO2是常用的一种防腐剂,其中+3价的N具有一定的氧化性。某实验小组利用以下反应2NO2+2NaOH=NaNO3+NaNO2+H2O制备NaNO2,并探究其性质。
I.制备NaNO2
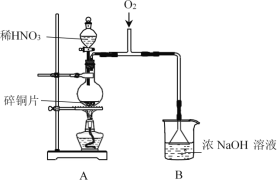
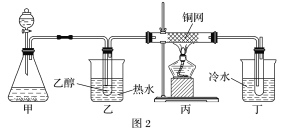
(1)A中发生反应的化学方程式是______。
(2)B中选用漏斗替代长直导管的优点是______。
(3)为检验B中制得NaNO2,甲进行以下实验:
序号 | 试管 | 操作 | 现象 |
① | 2mLB中溶液 | 加2mL0.1mol/LKI溶液,滴加几滴淀粉溶液 | 不变蓝 |
② | 2mLB中溶液 | 滴加几滴H2SO4至pH=5,加2mL0.1mol/LKI溶液,滴加几滴淀粉溶液 | 变蓝 |
③ | 2mLH2O | 滴加几滴H2SO4至pH=5,加2mL0.1mol/LKI溶液,滴加几滴淀粉溶液 | 不变蓝 |
实验③的目的是_______。
(4)乙认为上述3组实验无法证明B中一定含NaNO2,还需补充实验,理由是______。
II.探究NaNO2的性质
装置 | 操作 | 现象 |
| 取10mL1mol/LNaNO2溶液于试剂瓶中,加入几滴H2SO4酸化,再加入10mL1mol·L-1FeSO4溶液,迅速塞上橡胶塞,缓缓通入足量O2。 | i.溶液迅速变为棕色; ii.溶液逐渐变浅,有无色气泡产生,溶液上方为浅红棕色。 iii.最终形成棕褐色溶液。 |
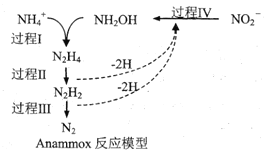
资料:i.
ii.HNO2在溶液中不稳定,易分解产生NO和NO2气体。
(5)现象i溶液变为棕色的原因是______。
(6)已知现象ii棕色溶液变浅是由于生成了Fe3+,反应的离子方程式是______。