题目内容
【题目】下列反应中,水作还原剂的是( )
A.2Na+2H2O=2NaOH+H2↑
B.CaO+H2O=Ca(OH)2
C.3NO2+H2O=2HNO3+NO
D.2F2+2H2O=4HF+O2
【答案】D
【解析】
A.在该反应中Na为还原剂,失去电子,H2O为氧化剂,获得电子变为H2,A不符合题意;
B.该反应中没有元素化合价的变化,属于非氧化还原反应,B不符合题意;
C.在该反应中只有NO2中的N元素的化合价发生变化,NO2既是氧化剂又是还原剂,C不符合题意;
D.在该反应中F2获得电子,为氧化剂,H2O中的O失去电子,H2O为还原剂,D符合题意;
故合理选项是D。

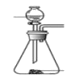
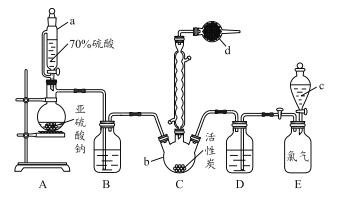
【题目】如图装置可用于收集SO2并验证其某些化学性质,下列说法正确的是

选项 | 试剂 | 现象 | 结论 |
A | 溴水 | 溶液褪色 | SO2有氧化性 |
B | H2S溶液 | 淡黄色沉淀 | SO2有氧化性 |
C | NaOH溶液 | 无明显现象 | SO2与NaOH溶液不反应 |
D | 紫色石蕊试液 | 溶液变红色后不褪色 | SO2有酸性、没有漂白性 |
A. A B. B C. C D. D
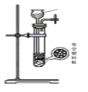
【题目】氯化亚砜(SOCl2)是一种液态化合物,沸点为 77℃,在农药、制药行业中用途广泛。SOCl2遇水剧烈反应,液面上产生白雾,并带有刺激性气味的气体产生.实验室合成原理:SO2+Cl2+SCl2═2SOCl2,部分装置如图所示,(已知 SCl2的沸点为 50℃).
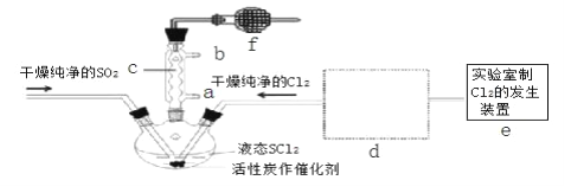
回答以下问题:
(1)下列四种制备 SO2的方案中最佳选择是____________________________
方案 | A | B | C | D |
发生装置 |
|
|
|
|
所选试剂 | 70%H2SO4+K2SO3 | 18.4mol/LH2SO4+Cu | 4mol/LHNO3+Na2SO3 | NaHCO3固体 |
(2)以 MnO2和浓盐酸为原料制备 Cl2的离子方程式为___________________________
(3)仪器 f 的作用是_________________________________________________
(4)d 的虚线框内隐含两个装置,按气流方向顺序这两个装置的药品分别是_______________。
(5)实验结束后,将三颈烧瓶混合物中产品分离出来的方法是 _________________________
(6)若用 SOCl2作 FeCl36H2O 的脱水剂,设计实验证明脱水时发生了氧化还原反应。取少量 FeCl36H2O 于试管中,加入过量 SOCl2,振荡,往试管中加水溶解,滴加____________或________溶液,证明脱水过程发生了氧化还原反应。