题目内容
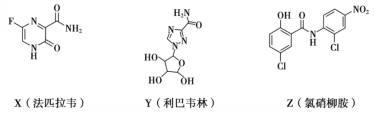
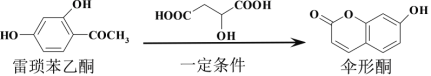
【题目】已知伞形酮可用雷琐苯乙酮和苹果酸在一定条件下反应制得,下列说法中正确的是
A.两分子苹果酸的一种缩合产物是:![]()
B.1mol雷琐苯乙酮最多能与3mol氢气发生加成反应
C.1mol产物伞形酮与溴水反应,最多可消耗3molBr2,均发生取代反应
D.反应中涉及到的三种有机物都能跟FeCl3溶液发生显色反应
【答案】A
【解析】
A.两分子苹果酸中,1个分子中的羟基与另一分子中的羧基酯化,同时该分子的1个羧基与另一分子中的羟基酯化,从而形成含有2个酯基的环酯:![]() ,A正确;
,A正确;
B.苯基与羰基都能与H2发生加成反应,则1mol雷琐苯乙酮最多能与4mol氢气发生加成反应,B不正确;
C.在伞形酮酚羟基的二个邻位上有氢原子,能与溴水发生取代反应,碳碳双键能与溴水发生加成反应,则1mol产物伞形酮与溴水反应,最多可消耗3molBr2,C不正确;
D.苹果酸不能跟FeCl3溶液发生显色反应,D不正确;
故选A。

 走进文言文系列答案
走进文言文系列答案【题目】草酸(H2C2O4)是一种二元弱酸,广泛分布于动植物体中。
(1)人体内草酸累积过多是导致结石(主要成分是草酸钙)形成的原因之一。有研究发现,EDTA(一种能结合金属离子的试剂)在一定条件下可以有效溶解结石,用化学平衡原理解释其原因:_______________。
(2)已知:0.1 mol·L-1KHC2O4溶液呈酸性。下列说法正确的是_______(填字母序号)。
a. 0.1 mol·L-1KHC2O4溶液中:c(K+) + c(H+) = c(HC2O4-) + 2c(C2O42-) + c(OH-)
b. 0.1 mol·L-1KHC2O4溶液中:c(K+) > c(HC2O4-) > c(C2O42-) > c(H2C2O4)
c. 浓度均为0.1 mol·L-1KHC2O4和K2C2O4的混合溶液中:2c(K+) = c(HC2O4-) + c(C2O42-)
d. 0.1 mol/L KHC2O4溶液中滴加等浓度NaOH溶液至中性:c(K+) > c(Na+)
(3)利用草酸制备草酸亚铁晶体(FeC2O4·xH2O)的流程及组分测定方法如下:
![]()
已知:i. pH>4时,Fe2+易被氧气氧化
ii. 几种物质的溶解度(g /100g H2O)如下
FeSO4·7H2O | (NH4)2SO4 | FeSO4·(NH4)2SO4·6H2O | |
20℃ | 48 | 75 | 37 |
60℃ | 101 | 88 | 38 |
①用稀硫酸调溶液pH至1~2的目的是:_____________,______________。
②趁热过滤的原因是:_______________。
③氧化还原滴定法常用于测定草酸亚铁晶体的摩尔质量(M)。称取a g草酸亚铁晶体溶于稀硫酸中,用b mol·L-1的高锰酸钾标准液滴定,到达滴定终点时,消耗高锰酸钾VmL,则M =__________。(已知:部分反应产物为Mn2+、Fe3+、CO2)
【题目】工业上可以用天青石生产碳酸锶后的含锶废渣制备高纯六水氯化锶(SrCl26H2O),含锶废渣主要成分为SrCO3,且含钡、铁、钙等元素。六水氯化锶是一种无色长针状晶体,易溶于水,微溶于无水乙醇和丙酮,下面为实验室模拟SrCl26H2O的制作流程:
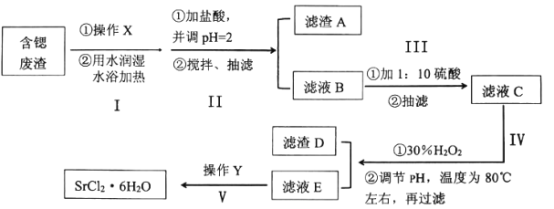
已知:①SrSO4微溶于水;
②SrCl26H2O在61.5℃以上即会失去4个结晶水生成SrCl22H2O。
(1)关于上述实验操作下列说法不正确的是___。
A.步骤I中操作X为研磨粉碎,可以增大反应接触面积
B.步骤III为提高产率,可以用滤液淋洗布氏漏斗中的滤渣
C.抽滤时,如果溶液有强酸性,可以用玻璃纤维代替滤纸
D.减压过滤不宜过滤胶状沉淀,因为胶状沉淀会在滤纸上形成一层密实的沉淀
E.步骤IV中的温度控制在80℃左右,可以用水浴加热,也可以用油浴或砂浴加热代替,更安全
(2)下表为实验中硫酸加入量对溶液中Ba2+和Sr2+含量的影响,实验发现在步骤III中加入硫酸量过量20%较合适,请解释原因:___。
硫酸加入量/mL | 4.50 | 4.95 | 5.40 | 5.85 | 6.30 |
Ba2+/(g/L) | 0.37 | 0.21 | 0.13 | 0.11 | 0.10 |
Sr2+/(g/L) | 90.21 | 89.86 | 89.57 | 89.23 | 88.90 |
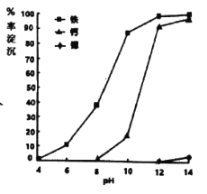
(3)①步骤IV调节pH时,为避免引入新的杂质,最适宜加入的试剂为___,如图为在80℃时,pH对除杂的影响,通过加入试剂将pH调至___。
②往滤渣D中加入NaClO溶液,发生反应的离子方程式为:___。
(4)在步骤V中,若要从滤液E通过操作Y得到大颗粒的高纯六水氯化锶晶体,操作Y包含下列步骤中的某几项,请选择合适的操作并排序。(填相应步骤的字母)
滤液E→(_____)→(_____)→(_____)→抽滤→(_____)→(_____)
a.蒸发浓缩至有大量晶体析出
b.在过饱和溶液中加入晶种
c.6l.5℃以上减压蒸发浓缩
d.6l.5℃以下减压蒸发浓缩
e.往溶液中加入无水乙醇
f.在30℃真空烘箱中干燥
g.在室温下缓慢冷却结晶
h.用氯化锶饱和溶液洗涤晶体
I.用冷水洗涤晶体
(5)为侧定所制SrCl26H2O晶体的纯度,取1.12g实验制得的产物加水溶解,配成100mL溶液,用移液管取出25mL于锥形瓶中,滴入几滴K2CrO4
①判断滴定终点的现象为___;
②实验时未采用棕色滴定管滴定,会使测得的晶体纯度___(填“偏高”、“偏低”或“不变”)。