题目内容
5.砷为第四周期ⅤA族元素,根据它在元素周期表中位置推测,砷不可能具有的性质是( )| A. | AsH3比NH3稳定 | B. | 可以存在-3、+3、+5等多种化合价 | ||
| C. | As2O5对应水化物的酸性比H3PO4弱 | D. | 砷的氧化性比磷弱 |
分析 D、根据同主族元素的元素从上到下元素的非金属性减弱来回答;
B、根据其最外层电子数结合同主族元素的元素周期律判断;
C、根据同主族元素的元素周期律判断该元素的非金属性强弱,再判断其氧化物的水化物的酸性强弱;
A、根据同主族元素的元素周期律判断该元素的非金属性强弱,再判断其氢化物的稳定性.
解答 解:A、N比砷的非金属性强,根据元素周期律知,NH3的稳定性比AsH3强,故A错误;
B、N元素有-3、0、+2、+3、+5等多种化合价,根据同主族元素的相似性判断,砷可以存在-3、+3、+5等多种化合价,故B正确;
C、磷比砷的非金属性强,根据元素周期律知,As2O5对应水化物的酸性比H3PO4弱,故C正确;
D、同主族元素的元素从上到下元素的非金属性减弱,所以砷的氧化性比磷弱,故D正确.
故选A.
点评 本题考查了元素周期律的应用,侧重考查学生对元素周期律的掌握程度.

练习册系列答案
相关题目
15.进行化学实验时应强化安全意识,下列做法正确的是( )
| A. | 金属钠着火时使用泡沫灭火器灭火 | |
| B. | 用试管加热碳酸氢钠固体时使试管口竖直向上 | |
| C. | 浓硫酸溅到皮肤上时立即用稀氢氧化钠溶液冲洗 | |
| D. | 少量金属汞洒落在实验室地面或桌面时,应立即向汞上撒硫黄粉,然后再清扫 |
16.下表中每组均有4个选项,请选出1个选项,它跟另外3个选项属于不同的分类,
| 组别 | 备选项 | 挑选项序号 |
| 1 | A.NO B.CO2 C.SO2 D.P2O5 | |
| 2 | A.S2- B.I-C.Fe D.K+ | |
| 3 | A.HCl B.CO2 C.NH3 D.Cl2 |
13.下列分子或离子的空间构型为平面三角形的是( )
| A. | NO${\;}_{3}^{-}$ | B. | NH3 | C. | H3O+ | D. | CO2 |
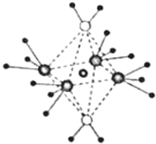 周期表前四周期的元素A、B、C、D、E,原子序数依次增大.A的核外电子总数与其周期数相同,B的价电子层中的未成对电子有3个,C的最外层电子数为其内层电子数的3倍,D与C同族;E的最外层只有1个电子,但次外层有18个电子.回答下列问题:
周期表前四周期的元素A、B、C、D、E,原子序数依次增大.A的核外电子总数与其周期数相同,B的价电子层中的未成对电子有3个,C的最外层电子数为其内层电子数的3倍,D与C同族;E的最外层只有1个电子,但次外层有18个电子.回答下列问题: .
.