题目内容
【题目】铁及铁的化合物应用广泛,如FeCl3可用作催化剂、印刷电路铜板腐蚀剂和外伤止血剂等。
(1)写出FeCl3溶液腐蚀印刷电路铜板的离子方程式_____________。
(2)若将(1)中的反应设计成原电池,请画出原电池的装置图,标出正、负极__________,并写出电极反应式。正极反应__________,负极反应____________。若用此电池向外电路输送0.5mol电子,负极质量_______(填增重或减轻)____克。
【答案】 2Fe3++Cu=2Fe2++Cu2+ 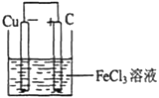 Fe3++e-=Fe2+(或2Fe3++2e-=2Fe2+) Cu-2e-=Cu2+ 减轻 16
Fe3++e-=Fe2+(或2Fe3++2e-=2Fe2+) Cu-2e-=Cu2+ 减轻 16
【解析】(1)Fe3+有强氧化性,能把金属铜氧化成铜离子,自身被还原成 Fe2+,反应方程式为2Fe3++Cu=2Fe2++Cu2+,故答案为:2Fe3++Cu=2Fe2++Cu2+;
(2)设计成原电池时,负极上发生氧化反应,正极上发生还原反应,该电池反应中三价铁离子得电子发生还原反应,所以正极上的电极反应式为Fe3++e-=Fe2+,铜失电子发生氧化反应,所以负极上的电极反应式为Cu-2e-=Cu2+;电池反应中发生氧化反应的金属作负极,所以铜作负极,不如负极活泼的金属或导电的非金属作正极,可选石墨作正极,发生还原反应的电解质溶液作原电池的电解质溶液,所以该原电池图为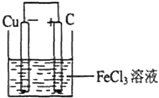 ,若用此电池向外电路输送0.5mol电子,负极溶解的铜为
,若用此电池向外电路输送0.5mol电子,负极溶解的铜为![]() =0.25mol,减少的质量为0.25mol×64g/mol=16g,故答案为:
=0.25mol,减少的质量为0.25mol×64g/mol=16g,故答案为:  ;Fe3++e-=Fe2+;Cu-2e-=Cu2+;减轻;16。
;Fe3++e-=Fe2+;Cu-2e-=Cu2+;减轻;16。

练习册系列答案
相关题目