题目内容
【题目】(1)一定条件下,某烷烃的密度是氢气密度的64倍,它有多种结构,写出其一氯代物有两种结构的该烷烃的结构简式___________。
(2)20mL某烃在80mL氧气中充分燃烧,反应后恢复至室温,混合气体体积变为50mL,则该烃的分子式为_______。
A.CH4 B.C3H6 C.C3H4 D.C2H6
(3)写出下列有机方程式:
①HOCH2CH2OH的催化氧化:__________。
②HOOCCOOH与HO CH2CH2OH酯化成环:____________。
③已知![]() +║→
+║→![]() 则,
则,![]() +
+![]() →___________。
→___________。
【答案】 (CH3)3CCH2C(CH3)3 D HOCH2CH2OH+O2![]() OHCCHO + 2H2O HOOCCOOH+HO CH2CH2OH
OHCCHO + 2H2O HOOCCOOH+HO CH2CH2OH![]()
![]() +2H2O
+2H2O ![]() +
+![]() →
→![]()
【解析】(1)因气体的密度之比等于摩尔质量之比,该烷烃蒸气的摩尔质量为2g/mol×64=128g/mol,则12n+2n+2=128,解得n=9,所以烷烃A的分子式为C9H20,其中一氯代物有两种结构,说明分子具有比较好的对称性,结构简式为(CH3)3CCH2C(CH3)3,故答案为:(CH3)3CCH2C(CH3)3;
(2)假定50mL气体全部为二氧化碳或二氧化碳和一氧化碳的混合气体,则烃分子中C原子数目为2.5,很明显不可能,说明氧气过量,则C原子数小于或等于2,令烃组成为CxHy,则:
CxHy+(x+![]() )O2
)O2![]() xCO2+
xCO2+![]() H2O,体积减少△V
H2O,体积减少△V
1 1+![]()
20mL 20mL+80mL-50mL=50mL
所以1:(1+![]() )=20mL:50mL,解得y=6,故选D。
)=20mL:50mL,解得y=6,故选D。
(3)①HOCH2CH2OH的催化氧化的化学方程式为HOCH2CH2OH+O2![]() OHCCHO + 2H2O,故答案为:HOCH2CH2OH+O2
OHCCHO + 2H2O,故答案为:HOCH2CH2OH+O2![]() OHCCHO + 2H2O;
OHCCHO + 2H2O;
②HOOCCOOH与HO CH2CH2OH酯化成环的化学方程式为HOOCCOOH+HO CH2CH2OH![]()
![]() +2H2O,故答案为:HOOCCOOH+HO CH2CH2OH
+2H2O,故答案为:HOOCCOOH+HO CH2CH2OH![]()
![]() +2H2O;
+2H2O;
③根据![]() +║→
+║→![]() ,
,![]() 和
和![]() 反应的化学方程式为
反应的化学方程式为![]() +
+![]() →
→![]() ,故答案为:
,故答案为:![]() +
+![]() →
→![]() 。
。

 阅读快车系列答案
阅读快车系列答案【题目】为验证氧化性Cl2 > Fe3+ > SO2,某小组用下图所示装置进行实验(夹持仪器和A中加热装置已略,气密性已检验)。
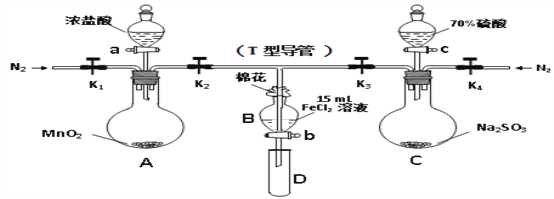
实验过程:
I.打开弹簧夹K1~K4,通入一段时间N2,再将T型导管插入B中, 继续通入N2,然后关闭K1、K3、K4。
Ⅱ.打开活塞a,滴加一定量的浓盐酸,加热A。
Ⅲ.当B中溶液变黄时,停止加热,夹紧K2。
Ⅳ.打开活塞b,使约2mL的溶液流入D试管中,并检验其中的离子。
Ⅴ.打开K3和活塞c,加入70%的硫酸,一段时间后夹紧K3。
Ⅵ.更新试管D,重复过程Ⅳ。
(1)过程Ⅰ的目的是_____________________________________________________。
(2)棉花中浸润的溶液为____________________________________________。
(3)A中发生反应的化学方程式为____________________________________________。
(4)能说明氧化性Fe3+ > SO2的离子方程式是__________________________________。
(5)过程Ⅵ,检验B溶液中是否含有SO42-的操作是________________________________。
(6)甲、乙、丙三位同学分别完成了上述实验,他们的检测结果不能够证明氧化性Cl2 > Fe3+ > SO2的是_______(填“甲”“乙”“丙”),请用必要的文字说明理由____________。
过程Ⅳ B溶液中含有的离子 | 过程Ⅵ B溶液中含有的离子 | |
甲 | 有Fe3+无Fe2+ | 有 Fe2+ |
乙 | 既有Fe3+又有Fe2+ | 有SO42- |
丙 | 有Fe3+无Fe2+ | 有SO42- |