题目内容
【题目】硼及其化合物的应用广泛。试回答下列问题:
(1)基态![]() 原子的价电子轨道表示式为__________,其第一电离能比
原子的价电子轨道表示式为__________,其第一电离能比![]() 的__________(填“大”或“小”)。
的__________(填“大”或“小”)。
(2)氨硼烷(![]() )被认为是最具潜力的新型储氢材料之一,分子中存在配位键,提供孤电子对的原子是__________,写出一种与氨硼烷互为等电子体的有机小分子:___________________(填化学式)。
)被认为是最具潜力的新型储氢材料之一,分子中存在配位键,提供孤电子对的原子是__________,写出一种与氨硼烷互为等电子体的有机小分子:___________________(填化学式)。
(3)常温常压下硼酸(![]() )的晶体结构为层状,其二维平面结构如图所示。
)的晶体结构为层状,其二维平面结构如图所示。
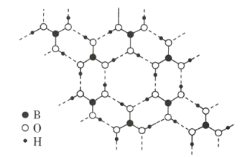
①B原子的杂化方式为__________。从氢键的角度解释硼酸在冷水中的溶解度小而加热时溶解度增大: _________________。
②路易斯酸碱理论认为,任何可接受电子对的分子或离子叫路易斯酸,任何可给出电子对的分子或离子叫路易斯碱。从结构角度分析硼酸是路易斯酸:______________________________。
【答案】![]() 小
小 ![]()
![]()
![]() 杂化硼酸分子间通过氢键缔合,加热时,部分氢键被破坏 硼酸分子中B原子有一个
杂化硼酸分子间通过氢键缔合,加热时,部分氢键被破坏 硼酸分子中B原子有一个![]() 空轨道
空轨道
【解析】
(1)![]() 、
、![]() 原子的核外电子排布式分别为
原子的核外电子排布式分别为![]() 、
、![]() ,
,![]() 原子的
原子的![]() 轨道处于全满状态,所以
轨道处于全满状态,所以![]() 的第一电离能比
的第一电离能比![]() 的小,
的小,![]() 原子的价电子轨道表示式为
原子的价电子轨道表示式为![]() ,故答案为:
,故答案为:![]() ;小。
;小。
(2)形成配位键,必须有一方提供空轨道,另一方提供孤对电子,在氨硼烷中,![]() 原子可提供一对孤电子,
原子可提供一对孤电子,![]() 原子有一个
原子有一个![]() 空轨道,
空轨道,![]() 与
与![]() 互为等电子体,故答案为:
互为等电子体,故答案为:![]() ;
;![]() 。
。
(3)①由图可知,硼酸中每个![]() 原子与
原子与![]() 原子形成3个
原子形成3个![]() 键,即
键,即![]() 原子有3个成键轨道,且没有孤电子对,故为
原子有3个成键轨道,且没有孤电子对,故为![]() 杂化,溶质分子间形成的氢键不利于溶质的溶解,加热时,硼酸的溶解度增大,可分析出,升温时硼酸分子中的部分氢键被破坏,故答案为:
杂化,溶质分子间形成的氢键不利于溶质的溶解,加热时,硼酸的溶解度增大,可分析出,升温时硼酸分子中的部分氢键被破坏,故答案为:![]() ;杂化硼酸分子间通过氢键缔合,加热时,部分氢键被破坏。
;杂化硼酸分子间通过氢键缔合,加热时,部分氢键被破坏。
②硼酸分子中,![]() 原子有一个空的
原子有一个空的![]() 轨道,可以接受电子对,根据路易斯酸碱理论可知,硼酸为路易斯酸,故答案为:硼酸分子中B原子有一个
轨道,可以接受电子对,根据路易斯酸碱理论可知,硼酸为路易斯酸,故答案为:硼酸分子中B原子有一个![]() 空轨道。
空轨道。

【题目】下表为元素周期表前四周期的一部分,下列有关X、Y、Z、R、W五种元素的叙述中,错误的是
X | ||||
Y | Z | |||
R | W |
A.常压下五种元素的单质中,Y的沸点最高
B.元素电负性:X>Z>Y
C.基态原子中未成对电子数最多的是R
D.元素最高价氧化物对应的水化物酸性:W>Z>Y
【题目】现有前四周期的5种元素的部分信息如下表所示:
元素代号 | 元素部分信息 |
X | X的阴离子核外电子云均呈球形 |
Y | 原子的最高能级上有3个未成对电子,其最简单气态氢化物在水中的溶解度在同族元素所形成的最简单气态氢化物中最大 |
Z | 基态原子核外有3个能级填充了电子,能量最高能级的电子数等于前两个能级的电子数之和 |
R | 元素原子的最外层电子排布式为nsn-1npn-1 |
T | 一种核素的质量数为65,中子数为36 |
根据上述元素信息,回答下列问题。
(1)基态T2+的电子排布式为__。
(2)Y、Z、R的电负性由大到小的顺序为__(用元素符号表示)。
(3)YX4+的空间构型为__,离子中![]() 原子的杂化轨道类型为___,YX4+的电子式为__。
原子的杂化轨道类型为___,YX4+的电子式为__。
(4)YX3的一种等电子体分子是__,YX3的键角大于X2Z的键角的主要原因是__。