题目内容
Q、W、X、Y、Z是原子序数依次增大的短周期元素,X、Y是金属元素,X的焰色呈黄色.五种元素核电荷数之和为54,最外层电子数之和为20.W、Z最外层电子数相同,Z的核电荷数是W的2倍.工业上一般通过电解氧化物的方法获得Y的单质.
(1)W、X、Y、Z原子半径由大到小的顺序(写元素符号):
(2)向X、Y和W三种元素形成的化合物的水溶液中通入过量QW2气体的反应的离子方程式为: .
(1)W、X、Y、Z原子半径由大到小的顺序(写元素符号):
(2)向X、Y和W三种元素形成的化合物的水溶液中通入过量QW2气体的反应的离子方程式为:
分析:X的焰色呈黄色,应为Na元素,X、Y是金属元素,且原子序数依次增大,则Y应为Al元素,W、Z最外层电子数相同,应为同主族元素,Z的核电荷数是W的2倍,可知W为O元素,Z为S元素,五种元素核电荷数之和为54,则Q的原子序数为54-8-16-11-13=6,应为C元素,据此解答.
解答:解:X的焰色呈黄色,应为Na元素,X、Y是金属元素,且原子序数依次增大,则Y应为Al元素,W、Z最外层电子数相同,应为同主族元素,Z的核电荷数是W的2倍,可知W为O元素,Z为S元素,五种元素核电荷数之和为54,则Q的原子序数为54-8-16-11-13=6,应为C元素,
(1)同周期自左而右原子半径减小,同主族自上而下原子半径增大,故原子半径Na>Al>S>O,
故答案为:Na>Al>S>O;
(2)X、Y和W三种元素形成的化合物为NaAlO2,向其水溶液中通入过量的二氧化碳,反应生成氢氧化铝沉淀和碳酸氢钠,反应离子方程式为AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-,
故答案为:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-.
(1)同周期自左而右原子半径减小,同主族自上而下原子半径增大,故原子半径Na>Al>S>O,
故答案为:Na>Al>S>O;
(2)X、Y和W三种元素形成的化合物为NaAlO2,向其水溶液中通入过量的二氧化碳,反应生成氢氧化铝沉淀和碳酸氢钠,反应离子方程式为AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-,
故答案为:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-.
点评:本题考查元素推断、原子半径比较、铝化合物性质,难度不大,推断元素是解题关键,(2)中注意二氧化碳过量.

练习册系列答案
 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案
相关题目
Q、W、X、Y、Z是原子序数依次增大的短周期元素,X的焰色反应呈黄色.Q元素的原子最外层电子数是其内层电子数的2倍.W、Z最外层电子数相同,Z的核电荷数是W的2倍.元素Y的合金是日常生活中使用广泛的金属材料之一,下列说法正确的是( )
| A、氢化物稳定性:Z>W | B、原子半径的大小顺序:rX>rY>rQ>rW | C、元素Q和Z能形成QZ2型的共价化合物 | D、X、Y的最高价氧化物的水化物之间不能发生反应 |
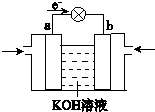 Q、W、X、Y、Z是5种短周期元素,原子序数逐渐增大,Q是周期表中原子半径最小的元素,Q与W组成的化合物是一种温室气体,W与Y、X与Y组成的化合物是机动车排出的大气污染物,Y和Z能形成原子个数比为1:1和1:2的两种离子化合物.
Q、W、X、Y、Z是5种短周期元素,原子序数逐渐增大,Q是周期表中原子半径最小的元素,Q与W组成的化合物是一种温室气体,W与Y、X与Y组成的化合物是机动车排出的大气污染物,Y和Z能形成原子个数比为1:1和1:2的两种离子化合物.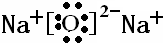

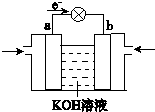
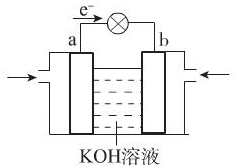 Q、W、X、Y、Z是5种短周期元素,原子序数逐渐增大;W与Q按1:4形成的化合物A是一种重要能源;W与Y,X与Y组成的化合物是常见的大气污染物;Y与Z按1:1形成的离子化合物B,其摩尔质量为78g?mol-1.请回答下列问题.
Q、W、X、Y、Z是5种短周期元素,原子序数逐渐增大;W与Q按1:4形成的化合物A是一种重要能源;W与Y,X与Y组成的化合物是常见的大气污染物;Y与Z按1:1形成的离子化合物B,其摩尔质量为78g?mol-1.请回答下列问题.