题目内容
【题目】高氯酸三碳酰肼合镍{[Ni(CHZ)3](C104)2}是一种新型的起爆药。
(1)Ni2+某杰核外电子排布式为________。
(2)ClO4空间构型是_______;与ClO4互为等电子体的一种分子为_______(填化学式)。
(3)化学式中CHZ为碳酰肼,组成为CO(N2H3)2,碳酰肼中碳原子的杂化轨道类型为_____;C、N、0三种元素的电负性由大到小的顺序为______。
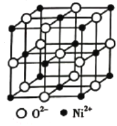
(4)高氯酸三碳酰肼合镍可由NiO、髙氯酸及碳酰肼化合而成。NiO的晶胞结构如图所示,晶胞中含有的Ni2+数目为_________。
【答案】[Ar]3d8 或1s22s22p63s23p63d8 正四面体 CCl4(SiF4等) sp2 O>N>C 4
【解析】
(1)Ni元素原子核外有28个电子,原子核外电子排布为1s22s22p63s23p63d84s2,Ni失去4s能级2个电子形成Ni2+;
(2)计算Cl原子价层电子对数、孤电子对,进而确定ClO4-的空间构型;原子总数相同、价电子总数相同的微粒互为等电子体;
(3)CO(N2H3)2中C原子与O原子之间形成双键,与N原子之间形成C-N单键,没有孤对电子,据此确定杂化轨道数目,进而确定杂化方式;元素的非金属性越强,电负性越大;
(4)Ni2+离子位于晶胞顶点及面心,可以均摊法计算晶胞中Ni2+数目。
(1)Ni元素原子核外有28个电子,原子核外电子排布为1s22s22p63s23p63d84s2,Ni失去4s能级2个电子形成Ni2+,Ni2+离子核外电子排布式为:1s22s22p63s23p63d8,;
(2)ClO4-中氯原子价层电子对数为4+![]() =4、没有孤电子对,故其空间构型是:正四面体;原子总数相同、价电子总数相同的微粒互为等电子体,与ClO4-互为等电子体的一种分子为CCl4等;
=4、没有孤电子对,故其空间构型是:正四面体;原子总数相同、价电子总数相同的微粒互为等电子体,与ClO4-互为等电子体的一种分子为CCl4等;
(3)CO(N2H3)2中C原子与O原子之间形成双键,与N原子之间形成C-N单键,没有孤对电子,杂化轨道数目为3,C原子采取sp2杂化;元素的非金属性越强,电负性越大,已知非金属性O>N>C,则C、N、0三种元素的电负性由大到小的顺序为O>N>C;
(4)Ni2+离子位于晶胞顶点及面心,晶胞中Ni2+数目=8×![]() +6×
+6×![]() =4。
=4。