题目内容
【题目】亚硝酸钠(NaNO2)是工业盐的主要成分,在漂白、电镀等方面应用广泛。实验室利用下图装置制备亚硝酸钠,并测定所制亚硝酸钠的纯度。(加热装置及部分夹持装置已略去)
Ⅰ.亚硝酸钠的制备。
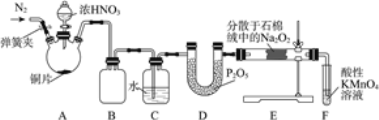
(1)盛放浓HNO3的仪器的名称为__________;装置B的作用是______________。
(2)装置E中制取NaNO2的化学方程式为___________________。
(3)多余的NO在装置F中被氧化为NO3-,反应的离子方程式为_____________。
(4)实验结束后打开A中弹簧夹,通入N2的目的是_______________。
Ⅱ.亚硝酸钠纯度的测定。
当Na2O2完全反应后,E中产生的固体除NaNO2外,还可能有NaNO3。测定亚硝酸钠纯度的步骤如下:
步骤一:取反应后的固体4.30 g溶于稀硫酸,向所得溶液中加入足量KI,将溶液中的NO2-和NO3-全部还原为NO,并通入足量N2,将NO全部赶出,最后将溶液稀释至1000 mL。
步骤二:取上述所得溶液10 mL,用淀粉作指示剂,用0.050 mol/L的Na2S2O3标准液滴定,发生的反应为I2+2Na2S2O3=2NaI+Na2S4O6,最终消耗Na2S2O3溶液体积为16.00 mL。
(5)步骤二中达到滴定终点的标志为______________________。
(6)混合固体中NaNO2的质量分数为________。(保留三位有效数字)
(7)若在滴定终点读取滴定管刻度时,仰视标准液液面,则测得亚硝酸钠的纯度________。(填“偏高”“偏低”或“无影响”)
【答案】分液漏斗 作安全瓶(防止液体倒吸) 2NO+Na2O2=2NaNO2 5NO+3MnO4-+4H+=5NO3-+3Mn2++2H2O 把装置内残留的NO驱赶至后续装置,使其充分吸收,避免污染空气 滴入最后一滴标准液后,溶液由蓝色褪为无色,且30 s内不再变化 80.2%(80.0%~80.3%即可) 偏低
【解析】
Cu与浓硝酸在装置A中反应产生NO2,随着反应的进行,当浓硝酸反应变为稀硝酸后,Cu与稀硝酸反应产生NO气体,装置B是安全瓶,气体经装置C,NO2会与水反应转化为HNO3和NO,NO气体经装置D中P2O5干燥后,在装置E中与Na2O2发生反应:2NO+Na2O2=2NaNO2,装置F是尾气处理装置,未反应的NO气体在装置F中被酸性高锰酸钾溶液氧化,防止污染环境。
(1)由装置图可知:盛放浓HNO3的仪器的名称为分液漏斗;装置B的作用是作安全瓶,防止液体倒吸。
(2)在装置E中NO与Na2O2发生反应NaNO2,反应的化学方程式为2NO+Na2O2=2NaNO2。
(3)装置F中多余的NO被酸性KMnO4氧化为NO3-,反应离子方程式为5NO+3MnO4-+4H+=5NO3-+3Mn2++2H2O。
(4)实验结束后,打开装置A中弹簧夹通入N2的目的是把装置内残留的NO驱赶至后续装置,使其充分吸收,避免污染空气。
(5)步骤二中以淀粉作指示剂,当达到滴定终点时,再滴入最后一滴标准液时,溶液由蓝色褪为无色,且30s内不再变化。
(6)步骤一将混合固体溶于稀硫酸,向所得溶液中加入足量KI,发生的反应方程式为4H++2NO2-+2I-=2NO↑+I2+2H2O和8H++2NO3-+6I-=2NO↑+3I2+4H2O,滴定过程发生的反应为I2+2Na2S2O3=2NaI+Na2S4O6,根据物料守恒,反应中Na2S2O3与I2的化学计量比为2∶1、I2与NO2-的化学计量比为1∶2、I2与NO3-反应的化学计量比为3∶2,则Na2S2O3与NO2-的化学计量比为1∶1、Na2S2O3与NO3-的化学计量比为3∶1,滴定消耗n(Na2S2O3)=0.050 mol·L-1×0.016 L=8.0×10-4 mol,设混合固体中NaNO2的质量分数为x,根据物料守恒得n(NaNO2)+3n(NaNO3)=n(Na2S2O3),则![]() mol=
mol=![]() ×8.0×10-4mol,解得x=0.802,所以混合固体中NaNO2的质量分数为80.2%(80.0%~80.3%即可)。
×8.0×10-4mol,解得x=0.802,所以混合固体中NaNO2的质量分数为80.2%(80.0%~80.3%即可)。
(7)若在滴定终点读取滴定管刻度时,仰视标准液液面,则滴定读数偏大,计算所得硝酸钠偏多,则测得亚硝酸钠的纯度偏低。

【题目】下列根据实验操作和现象所得出的结论错误的是
选项 | 实验操作 | 实验现象 | 结论 |
A | 向溶液X中先滴加稀硝酸,再滴加Ba(NO3)2溶液 | 出现白色沉淀 | 溶液X不一定含有SO42- |
B | 向FeCl3+3KSCN | 体系颜色无变化 | KCl不能使该平衡移动 |
C | 向浓度均为0.1mol·L-1NaOH和NaI混合溶液中滴加少量AgNO3溶液 | 出现黄色沉淀 | Ksp(AgCl)>Ksp(AgI) |
D | 向两份蛋白质溶液中分别滴加饱和NaCl溶液和CuSO4溶液 | 均有固体析出 | 蛋白质均发生变性 |
A.AB.BC.CD.D