题目内容
反应4NH3+5O2 4NO+6H2O在5 L密闭容器中进行,半分钟后,NO的物质的量增加了0.3 mol,则此反应的平均速率
4NO+6H2O在5 L密闭容器中进行,半分钟后,NO的物质的量增加了0.3 mol,则此反应的平均速率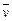 (X)(表示反应物的消耗速率或生成物的生成速率)为
(X)(表示反应物的消耗速率或生成物的生成速率)为
 4NO+6H2O在5 L密闭容器中进行,半分钟后,NO的物质的量增加了0.3 mol,则此反应的平均速率
4NO+6H2O在5 L密闭容器中进行,半分钟后,NO的物质的量增加了0.3 mol,则此反应的平均速率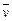 (X)(表示反应物的消耗速率或生成物的生成速率)为
(X)(表示反应物的消耗速率或生成物的生成速率)为A.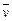 (O2)=0.01 mol·L-1·s-1 (O2)=0.01 mol·L-1·s-1 |
B.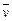 (NO)=0.008 mol·L-1·s-1 (NO)=0.008 mol·L-1·s-1 |
C.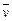 (H2O)=0.003 mol·L-1·s-1 (H2O)=0.003 mol·L-1·s-1 |
D.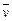 (NH3)=0.002 mol·L-1·s-1 (NH3)=0.002 mol·L-1·s-1 |
CD
反应的平均速率是指单位时间内某物质浓度的变化量。已知容器体积为5 L,时间半分钟即30 s,NO的物质的量(变化量)为0.3 mol,则c(NO)=0.3 mol/5 L=0.06 mol·L-1。
所以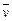 (NO)=0.06 mol·L-1/30 s=0.002 mol·L-1·s-1。即可求出:
(NO)=0.06 mol·L-1/30 s=0.002 mol·L-1·s-1。即可求出:
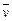 (O2)=0.002 mol·L-1·s-1×
(O2)=0.002 mol·L-1·s-1×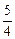 =0.0025 mol·L-1·s-1;
=0.0025 mol·L-1·s-1;
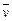 (H2O)=0.002 mol·L-1·s-1×
(H2O)=0.002 mol·L-1·s-1×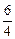 =0.003 mol·L-1·s-1;
=0.003 mol·L-1·s-1;
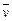 (NH3)=0.002 mol·L-1·s-1×
(NH3)=0.002 mol·L-1·s-1×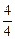 =0.002 mol·L-1·s-1。
=0.002 mol·L-1·s-1。
所以
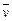 (NO)=0.06 mol·L-1/30 s=0.002 mol·L-1·s-1。即可求出:
(NO)=0.06 mol·L-1/30 s=0.002 mol·L-1·s-1。即可求出: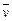 (O2)=0.002 mol·L-1·s-1×
(O2)=0.002 mol·L-1·s-1×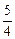 =0.0025 mol·L-1·s-1;
=0.0025 mol·L-1·s-1;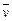 (H2O)=0.002 mol·L-1·s-1×
(H2O)=0.002 mol·L-1·s-1×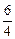 =0.003 mol·L-1·s-1;
=0.003 mol·L-1·s-1;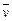 (NH3)=0.002 mol·L-1·s-1×
(NH3)=0.002 mol·L-1·s-1×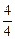 =0.002 mol·L-1·s-1。
=0.002 mol·L-1·s-1。
练习册系列答案
相关题目
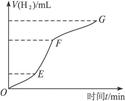
 2NH3的反应中,各物质的起始浓度分别为:c(H2)="4" mol·L-1,c(N2)="3" mol·L-1,c(NH3)="0.5" mol·L-1,经3 min后,c(NH3)="0.8" mol·L-1,该反应的反应速率是( )
2NH3的反应中,各物质的起始浓度分别为:c(H2)="4" mol·L-1,c(N2)="3" mol·L-1,c(NH3)="0.5" mol·L-1,经3 min后,c(NH3)="0.8" mol·L-1,该反应的反应速率是( )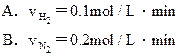
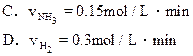
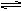 2HI,反应进行到2min时测得反应速率υ(HI)=0.1mol/(L·min),I2(g)的物质的量浓度为0.4mol/L。
2HI,反应进行到2min时测得反应速率υ(HI)=0.1mol/(L·min),I2(g)的物质的量浓度为0.4mol/L。 4C(?)+2D(?)。反应一段时间后达到平衡,测得生成1.6 mol C,且反应的前后压强之比为5:4(相同的温度下测量),则下列说法正确的是( )
4C(?)+2D(?)。反应一段时间后达到平衡,测得生成1.6 mol C,且反应的前后压强之比为5:4(相同的温度下测量),则下列说法正确的是( )