题目内容
100 mL 2 mol/L H2SO4与过量Zn粉反应,在一定温度下,为了加快反应速率,但又不影响生成氢气的总量,可以采取的措施是( )
| A.加入碳酸钠固体 | B.改用18 mol/L的浓H2SO4 |
| C.滴入少量硫酸铜溶液 | D.加入硫酸钾溶液 |
C
解析试题分析::A、加入碳酸钠固体会和硫酸中的氢离子之间反应生成二氧化碳气体,氢离子浓度减小,速率减慢,且影响生成氢气的量,故A错误;B、改用18mol/L的浓H2SO4,则金属锌和浓硫酸之间反应不会产生氢气,产生的是二氧化硫,故B错误;C、加入少量的CuSO4溶液,锌置换出铜形成铜、锌原电池反应,反应速率增大,且氢气的总量不变,故C正确;D、加入硫酸钾溶液,相当于加入水,体积增大,氢离子的浓度减小,反应速率减慢,故D错误。
考点:考查化学反应速率的影响因素。

练习册系列答案
 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案
相关题目
一定温度下,在2 L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如下图所示。下列描述正确的是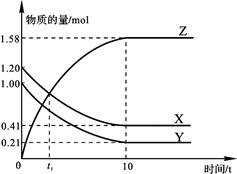
| A.反应开始到10 s,用Z表示的反应速率为0.158 mol/(L·s) |
| B.反应开始到10 s时,Y的转化率为79.0% |
| C.t1时,Z和X的浓度相等,达到了化学平衡状态 |
D.反应的化学方程式为:X(g)+Y(g) Z(g) Z(g) |
汽车尾气中的有毒气体NO和CO,在一定条件下可发生反应生成N2和CO2。下列关于此反应的说法中,正确的是( )
| A.减小压强能增大反应速率 | B.增大压强能减小反应速率 |
| C.使用适当的催化剂能增大反应速率 | D.升高温度对反应速率无影响 |
在C(s)+CO2(g)===2CO(g)的反应中,现采取下列措施:
①缩小体积,增大压强 ②增加碳的量 ③通入CO2 ④恒容下充入N2
⑤恒压下充入N2能够使反应速率增大的措施是( )
| A.①④ | B.②③⑤ | C.①③ | D.①②④ |
一定条件下,水蒸气含量随反应时间的变化趋势符合下图的是( )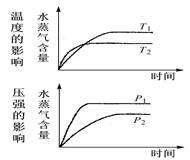
A.CO2(g)+2NH3( g) CO(NH2)2(s)+H2O(g); △H<0 CO(NH2)2(s)+H2O(g); △H<0 |
B.CO2(g)+ H2(g)  CO(g)+H2O(g); △H>0 CO(g)+H2O(g); △H>0 |
C.CH3CH2OH CH2=CH2(g)+ H2O(g); △H>0 CH2=CH2(g)+ H2O(g); △H>0 |
D.2C6H5CH2CH3(g)+O2(g) 2C6H-5CH=CH2(g)+2H2O(g); △H<0 2C6H-5CH=CH2(g)+2H2O(g); △H<0 |
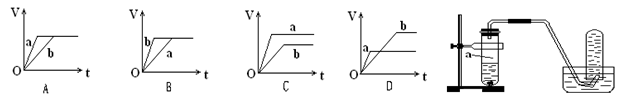
T ℃时在2L容积不变的密闭容器中使X(g)与Y(g)发生反应生成Z(g)。反应过程中X、Y、Z 的 浓度变化如图1所示;若保持其他条件不变,温度分别为T1和T2时,Y的体积百分含量与时间的关系如图2所示。则下列结论错误的是
A.容器中发生的反应可表示为:3X(g)+Y(g) 2Z(g) 2Z(g) |
| B.反应进行前3min内,用X表示的反应速率v(X)=0.1mol/(L·min) |
| C.若改变反应条件,使反应进程如图3所示,则改变的条件是使用催化剂 |
| D.保持其他条件不变,升高温度,化学平衡向逆反应方向移动 |
 2C(气)达到平衡的标志是
2C(气)达到平衡的标志是