题目内容
5.下列有关物质的表达式不正确的是( )| A. | 乙烯的结构简式:CH2 CH2 | B. | CS2分子的结构式:S═C═S | ||
| C. | 醛基的结构简式:-CHO | D. | 羟基的电子式:${\;}_{\;}^{•}$$\underset{\stackrel{••}{O}}{••}$${\;}_{•}^{•}$H |
分析 A.乙烯的最简式中没有标出其官能团碳碳双键;
B.二硫化碳的结构式与二氧化碳类似,分子中存在两个共价键;
C.醛基中存在1个碳氢键和1个碳氧双键,为中性原子团;
D.羟基为中性原子团,存在1个氧氢键,氧原子最外层为7个电子.
解答 解:A.乙烯含有官能团碳碳双键,结构简式中必须标出官能团,乙烯正确的最简式为CH2=CH2,故A错误;
B.CS2分子中存在两个碳硫双键,其结构式为:S═C═S,故B正确;
C.醛基为醛类的官能团,醛基的结构简式为:-CHO,故C正确;
D.氧原子与氢原子通过一对共用电子对连接,羟基中的氧原子含有一个未成对电子,电子式为: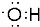 ,故D正确;
,故D正确;
故选A.
点评 本题考查了结构式、结构简式、电子式等化学用语的判断,题目难度中等,注意掌握常见化学用语的概念及表示方法,明确结构简式与结构式、电子式的区别,试题培养了学生灵活应用所学知识的能力.

练习册系列答案
相关题目
15.下列说法中,正确的是( )
| A. | 配制溶液定容时俯视刻度线将使所配溶液浓度偏低 | |
| B. | 18g H2O在标准状况下的体积为22.4L | |
| C. | 在标准状况下,20mLNH3 与60mLO2所含的分子数比为1:3 | |
| D. | 将40g NaOH溶于1L水中,所得溶液的物质的量浓度为1mol/L |
13.Ⅰ.常温下,将某一元酸HA(甲、乙、丙、丁代表不同的一元酸)和NaOH溶液等体积混合,两种溶液的物质的量浓度和混合溶液的pH如表所示:
(1)从甲组情况分析,如何判断HA是强酸还是弱酸?a=7时,HA是强酸;a>7时,HA是弱酸.
(2)乙组混合溶液中c(A-)和c(Na+)的大小关系是C.
A.前者大 B.后者大
C.二者相等 D.无法判断
(3)从丙组实验结果分析,该混合溶液中离子浓度由大到小的顺序是c(Na+)>c(A-)>c(OH-)>c(H+).
(4)分析丁组实验数据,写出该混合溶液中下列算式的精确结果(列式):c(Na+)-c(A-)=10-4-10-10 mol/L.
Ⅱ.某二元酸(化学式用H2B表示)在水中的电离方程式是:H2B═H++HB-,HB-?H++B2-.
(5)在0.1mol/L的Na2B溶液中,下列粒子浓度关系式正确的是AC.
A.c(B2-)+c(HB-)=0.1mol/L
B.c(B2-)+c(HB-)+c(H2B)=0.1mol/L
C.c(OH-)=c(H+)+c(HB-)
D.c(Na+)+c(OH-)=c(H+)+c(HB-)
| 实验编号 | HA的物质的量浓度(mol/L) | NaOH的物质的量浓度(mol/L) | 混合后溶液的pH |
| 甲 | 0.1 | 0.1 | pH=a |
| 乙 | 0.12 | 0.1 | pH=7 |
| 丙 | 0.2 | 0.1 | pH>7 |
| 丁 | 0.1 | 0.1 | pH=10 |
(2)乙组混合溶液中c(A-)和c(Na+)的大小关系是C.
A.前者大 B.后者大
C.二者相等 D.无法判断
(3)从丙组实验结果分析,该混合溶液中离子浓度由大到小的顺序是c(Na+)>c(A-)>c(OH-)>c(H+).
(4)分析丁组实验数据,写出该混合溶液中下列算式的精确结果(列式):c(Na+)-c(A-)=10-4-10-10 mol/L.
Ⅱ.某二元酸(化学式用H2B表示)在水中的电离方程式是:H2B═H++HB-,HB-?H++B2-.
(5)在0.1mol/L的Na2B溶液中,下列粒子浓度关系式正确的是AC.
A.c(B2-)+c(HB-)=0.1mol/L
B.c(B2-)+c(HB-)+c(H2B)=0.1mol/L
C.c(OH-)=c(H+)+c(HB-)
D.c(Na+)+c(OH-)=c(H+)+c(HB-)
10.有甲、乙、丙三种物质:
甲: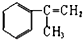 乙:
乙: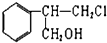
(1)关于乙下列叙述正确的是bd
a.1mol该有机物在加热和催化剂作用下,最多能和2mol NaOH反应
b.该有机物能使酸性KMnO4溶液褪色
c.该有机物的分子式为C9H11Cl
d.该有机物在一定条件下,能发生消去反应、取代反应、氧化反应和还原反应
(2)由甲转化为乙需经下列过程(已略去各步反应的无关产物,下同):
甲$→_{Ⅰ}^{一定条件}$ $→_{Ⅱ}^{一定条件}$Y$→_{Ⅲ}^{一定条件}$乙
$→_{Ⅱ}^{一定条件}$Y$→_{Ⅲ}^{一定条件}$乙
①反应Ⅰ的反应条件是光照
②其中反应II的化学方程式是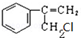 +NaOH$→_{△}^{H_{2}O}$
+NaOH$→_{△}^{H_{2}O}$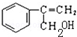 +NaCl
+NaCl
(3)由甲出发合成丙的路线之一如图:

①写出反应②的化学方程式
②写出C与丙的结构简式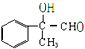 、
、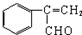 .
.
甲:
 乙:
乙: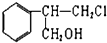
| 丙分子式 | C9H8O |
| 部分性质 | 能使Br2/CCl4褪色 |
a.1mol该有机物在加热和催化剂作用下,最多能和2mol NaOH反应
b.该有机物能使酸性KMnO4溶液褪色
c.该有机物的分子式为C9H11Cl
d.该有机物在一定条件下,能发生消去反应、取代反应、氧化反应和还原反应
(2)由甲转化为乙需经下列过程(已略去各步反应的无关产物,下同):
甲$→_{Ⅰ}^{一定条件}$
 $→_{Ⅱ}^{一定条件}$Y$→_{Ⅲ}^{一定条件}$乙
$→_{Ⅱ}^{一定条件}$Y$→_{Ⅲ}^{一定条件}$乙①反应Ⅰ的反应条件是光照
②其中反应II的化学方程式是
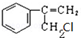 +NaOH$→_{△}^{H_{2}O}$
+NaOH$→_{△}^{H_{2}O}$ +NaCl
+NaCl(3)由甲出发合成丙的路线之一如图:

①写出反应②的化学方程式

②写出C与丙的结构简式
 、
、 .
.
17.下列说法正确的是( )
| A. | 硅酸钠溶液就是建筑行业中常用的黏合剂“水玻璃” | |
| B. | 工艺师利用盐酸刻蚀石英制作艺术品 | |
| C. | 水晶项链和餐桌上的瓷盘都是硅酸盐制品 | |
| D. | 粗硅制备单晶硅不涉及氧化还原反应 |
14.分析如图的能量变化示意图,确定下列热化学方程式书写正确的是( )
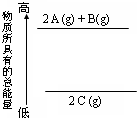

| A. | 2A+B=2C△H<0 | B. | 2C(g)=2A(g)+B(g)△H<0 | ||
| C. | 2 A(g)+B(g)=2C(g);△H>0 | D. | 2A(g)+B(g)=2C(g);△H<0 |
15.下列说法正确的是( )
| A. | CH3COOH与NaOH在相同条件下电离程度相等 | |
| B. | NaCl溶液能导电是因为溶液中有自由移动的Na+和Cl- | |
| C. | H2SO4在电流作用下在水中电离出H+和SO42- | |
| D. | 检验CO32-和HCO3-离子的方法是取少量样品加入盐酸,将产生的气体通入石灰水 |
