题目内容
某工厂用FeCl3溶液腐蚀镀有铜的绝缘板生产印刷电路.某实验小组的同学对该厂生产印刷电路后所得的废液进行了分析:取50mL废液,向其中加入足量的稀硝酸,生成0.02mol NO;另取50mL废液,向其中加入足量的AgNO3溶液,析出沉淀43.05g.
请回答下列问题:
(1)该厂原来使用的FeCl3溶液中溶质的物质的量浓度为(反应前后溶液的体积变化忽略不计).
(2)原废液中各金属阳离子的物质的量浓度之比为.
(3)另取50mL废液,加入一定量铁屑,充分反应后有铜析出,则所得溶液中Fe2+的物质的量范围为.
请回答下列问题:
(1)该厂原来使用的FeCl3溶液中溶质的物质的量浓度为(反应前后溶液的体积变化忽略不计).
(2)原废液中各金属阳离子的物质的量浓度之比为.
(3)另取50mL废液,加入一定量铁屑,充分反应后有铜析出,则所得溶液中Fe2+的物质的量范围为.
考点:化学方程式的有关计算,硝酸的化学性质,铁盐和亚铁盐的相互转变
专题:计算题
分析:(1)废液加入足量的AgNO3溶液,生成沉淀43.05g为AgCl质量,根据氯元素守恒计算溶液中n(FeCl3),根据c=
计算原废液中c(FeCl3);
(2)废液中加入硝酸发生反应:3Fe2++4H++NO3-=3Fe3++NO↑+2H2O,根据NO计算废液中n(Fe2+),再根据2Fe3++Cu=2Fe2++Cu2+,计算溶液中n(Cu2+)、参加反应Fe3+物质的量,进而计算废液中n(Fe3+),离子浓度之比等于物质的量之比;
(3)刚开始析出Cu时溶液中Fe2+的物质的量最小,Fe3+完全反应,发生反应:2Fe3++Fe=3Fe2+,Cu恰好完全析出时,溶液中Fe2+的物质的量最大,发生反应Cu2++Fe=Fe2++Cu,由(2)中数据结合方程式计算.
| n |
| V |
(2)废液中加入硝酸发生反应:3Fe2++4H++NO3-=3Fe3++NO↑+2H2O,根据NO计算废液中n(Fe2+),再根据2Fe3++Cu=2Fe2++Cu2+,计算溶液中n(Cu2+)、参加反应Fe3+物质的量,进而计算废液中n(Fe3+),离子浓度之比等于物质的量之比;
(3)刚开始析出Cu时溶液中Fe2+的物质的量最小,Fe3+完全反应,发生反应:2Fe3++Fe=3Fe2+,Cu恰好完全析出时,溶液中Fe2+的物质的量最大,发生反应Cu2++Fe=Fe2++Cu,由(2)中数据结合方程式计算.
解答:
解:(1)废液加入足量的AgNO3溶液,生成沉淀43.05g为AgCl质量,其物质的量=
=0.3mol,根据氯元素守恒,原溶液中n(FeCl3)=
n(AgCl)=
×0.3mol=0.1mol,故原废液中c(FeCl3)=
=2mol/L,
答:FeCl3溶液中溶质的物质的量浓度为2mol/L.
(2)由3Fe2++4H++NO3-=3Fe3++NO↑+2H2O,可知废液中n(Fe2+)=3n(NO)=0.02mol×3=0.06mol,根据2Fe3++Cu=2Fe2++Cu2+,可知溶液n(Cu2+)=
n(Fe2+)=
×0.06mol=0.03mol、参加反应Fe3+物质的量=n(Fe2+)=0.06mol,故废液中n(Fe3+)=0.1mol-0.06mol=0.04mol,离子浓度之比等于物质的量之比,故c(Fe3+):c(Fe2+):c(Cu2+)=0.04mol:0.06mol:0.03mol=4:6:3,
答:废液中各阳离子浓度之比为c(Fe3+):c(Fe2+):c(Cu2+)=4:6:3.
(3)刚开始析出Cu时溶液中Fe2+的物质的量最小,Fe3+完全反应,则:
2Fe3++Fe=3Fe2+
0.04mol 0.06mol
故Fe2+的物质的量极小值为0.06mol+0.06mol=0.12mol,由于析出Cu,故Fe2+的物质的量最小大于0.12mol,
Cu恰好完全析出时,溶液中Fe2+的物质的量最大,则:
Cu2++Fe=Fe2++Cu
0.03mol 0.03mol
故溶液中Fe2+的物质的量最大为0.12mol+0.03mol=0.15mol,
故溶液中0.12mol<n(Fe2+)≤0.15mol,
答:溶液中0.12mol<n(Fe2+)≤0.15mol.
| 43.05g |
| 143.5g/mol |
| 1 |
| 3 |
| 1 |
| 3 |
| 0.1mol |
| 0.05L |
答:FeCl3溶液中溶质的物质的量浓度为2mol/L.
(2)由3Fe2++4H++NO3-=3Fe3++NO↑+2H2O,可知废液中n(Fe2+)=3n(NO)=0.02mol×3=0.06mol,根据2Fe3++Cu=2Fe2++Cu2+,可知溶液n(Cu2+)=
| 1 |
| 2 |
| 1 |
| 2 |
答:废液中各阳离子浓度之比为c(Fe3+):c(Fe2+):c(Cu2+)=4:6:3.
(3)刚开始析出Cu时溶液中Fe2+的物质的量最小,Fe3+完全反应,则:
2Fe3++Fe=3Fe2+
0.04mol 0.06mol
故Fe2+的物质的量极小值为0.06mol+0.06mol=0.12mol,由于析出Cu,故Fe2+的物质的量最小大于0.12mol,
Cu恰好完全析出时,溶液中Fe2+的物质的量最大,则:
Cu2++Fe=Fe2++Cu
0.03mol 0.03mol
故溶液中Fe2+的物质的量最大为0.12mol+0.03mol=0.15mol,
故溶液中0.12mol<n(Fe2+)≤0.15mol,
答:溶液中0.12mol<n(Fe2+)≤0.15mol.
点评:本题考查混合物计算、化学方程式计算,题目难度中等,明确发生的反应是关键,(3)中注意根据离子氧化性强弱确定极值点,有利于培养学生的分析、理解能力及灵活应用所学知识的能力.

练习册系列答案
相关题目
如果n为第ⅡA族中某元素的原子序数,则原子序数为(n+1)的元素可能位于( )
| A、ⅢA或ⅢB | B、ⅣA |
| C、ⅠB | D、ⅠA |
下列化合物能发生消去反应生成烯烃,又能发生水解反应的是( )
①CH3Cl ② ③
③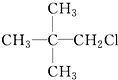 ④CH3CH2CH2Br.
④CH3CH2CH2Br.
①CH3Cl ②
 ③
③ ④CH3CH2CH2Br.
④CH3CH2CH2Br.| A、①③ | B、②④ | C、①④ | D、②③ |
下列物质在一定条件下,不能和氢气发生加成反应的是( )
| A、乙醛 | B、丙酮 | C、乙酸 | D、甲苯 |