题目内容
(1)某有机物A的质量为9.2克,完全燃烧后生成0.4mol二氧化碳和10.8克水,且此有机物的蒸气的相对密度是相同状况下氢气的23倍,求:
①此有机物的分子式为
②写出该有机物可能的结构简式
(2)某烃B的相对分子质量为84.回答下列问题:
①若链烃B分子中所有的碳原子共平面,该分子的一氯取代物只有一种,则B的结构简式为 .
②若烃B不能使溴水褪色,并且其一氯代物只有一种,则B的结构简式为 .
①此有机物的分子式为
②写出该有机物可能的结构简式
(2)某烃B的相对分子质量为84.回答下列问题:
①若链烃B分子中所有的碳原子共平面,该分子的一氯取代物只有一种,则B的结构简式为
②若烃B不能使溴水褪色,并且其一氯代物只有一种,则B的结构简式为
考点:有关有机物分子式确定的计算,有机物实验式和分子式的确定
专题:计算题,有机化学基础
分析:(1)根据有机物A的蒸气相对氢气的密度可计算其相对分子质量,进而求得9.2克有机物的物质的量,根据CO2和H2O的质量判断9.2克有机物中是否含有O元素,并计算O原子的质量,进而计算C、H、O的物质的量比值,结合相对分子质量可得该有机物的化学式,并书写结构简式;
(2)某烃B的相对分子质量为84,分子中C原子数目最大值=
=7,故分子式为C6H12,
①烃B为链烃,分子中所有的碳原子在同一平面上,含有C=C双键,该分子的一氯取代物只有一种,则结构对称,只含一种H,故含有4个甲基;
②烃B不能使溴水,褪色,且其一氯代物只有一种,则不含C=C,只有一种H,应为环烷烃.
(2)某烃B的相对分子质量为84,分子中C原子数目最大值=
| 84 |
| 12 |
①烃B为链烃,分子中所有的碳原子在同一平面上,含有C=C双键,该分子的一氯取代物只有一种,则结构对称,只含一种H,故含有4个甲基;
②烃B不能使溴水,褪色,且其一氯代物只有一种,则不含C=C,只有一种H,应为环烷烃.
解答:
解:(1)①n(CO2)=0.4mol,则2.3g有机物中:n(C)=n(CO2)=0.4mol,m(C)=0.4mol×12g/mol=4.8g,
n(H2O)=
=0.6mol,则9.2g有机物中:n(H)=2n(H2O)=1.2mol,m(H)=1.2mol×1g/mol=1.2g,
因(1.2g+4.8g)=6g<9.2g,所以有机物A中还有O元素,且m(O)=9.2g-4.8g-1.2g=3.2g,n(O)=
=0.2mol,
则有机物中:n(C):n(H):n(O)=0.4mol:1.2mol:0.2mol=2:6:1,所以该有机物的最简式为C2H6O,
又该化合物的蒸气对氢气的相对密度是23,则M=2×23=46,而C2H6O的相对分子质量为46,所以该有机物的分子式为C2H6O,
故答案为:C2H6O;
②分子式为C2H6O的有机物可以为乙醇或二甲醚,结构简式为:CH3CH2OH或CH3OCH3,
故答案为:C2H5OH或CH3OCH3;
(2)烃B的相对分子质量为84,分子中C原子数目最大值=
=7,故分子式为C6H12,
①烃B为链烃,分子中所有的碳原子在同一平面上,含有C=C双键,该分子的一氯取代物只有一种,则结构对称,只含一种H,即含4个甲基,A为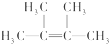 ,
,
故答案为: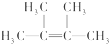 ;
;
②烃B不能使溴水褪色,且其一氯代物只有一种,则不含C=C,只有一种H,应为环烃,其结构简式为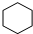 ,
,
故答案为: .
.
n(H2O)=
| 10.8g |
| 18g/mol |
因(1.2g+4.8g)=6g<9.2g,所以有机物A中还有O元素,且m(O)=9.2g-4.8g-1.2g=3.2g,n(O)=
| 3.2g |
| 16g/mol |
则有机物中:n(C):n(H):n(O)=0.4mol:1.2mol:0.2mol=2:6:1,所以该有机物的最简式为C2H6O,
又该化合物的蒸气对氢气的相对密度是23,则M=2×23=46,而C2H6O的相对分子质量为46,所以该有机物的分子式为C2H6O,
故答案为:C2H6O;
②分子式为C2H6O的有机物可以为乙醇或二甲醚,结构简式为:CH3CH2OH或CH3OCH3,
故答案为:C2H5OH或CH3OCH3;
(2)烃B的相对分子质量为84,分子中C原子数目最大值=
| 84 |
| 12 |
①烃B为链烃,分子中所有的碳原子在同一平面上,含有C=C双键,该分子的一氯取代物只有一种,则结构对称,只含一种H,即含4个甲基,A为
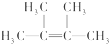 ,
,故答案为:
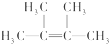 ;
;②烃B不能使溴水褪色,且其一氯代物只有一种,则不含C=C,只有一种H,应为环烃,其结构简式为
 ,
,故答案为:
 .
.
点评:本题考查有机物分子式确定、限制条件同分异构体的书写,难度中等,注意掌握燃烧法利用原子守恒确定有机物组成.

练习册系列答案
 轻巧夺冠周测月考直通中考系列答案
轻巧夺冠周测月考直通中考系列答案
相关题目
能大量共存于同一溶液中,在该溶液中加入过量的NaOH溶液或适量稀硫酸,都可能产生白色沉淀的离子组是( )
| A、NH4+ Ba2+ Fe3+ Cl- |
| B、Ba2+ Mg2+ NO3- Ca2+ |
| C、H+ Ba2+ Al3+ Cl- |
| D、K+ Ca2+ OH- HCO3- |
一定温度下固定体积的密闭容器中发生下列反应:2HI?H2+I2.若c(HI)由0.1mol?L-1降到0.07mol?L-1时,需要15s,那么c(HI)由0.07mol?L-1降到0.05mol?L-1时,所需反应的时间为( )
| A、5s | B、10s |
| C、大于10s | D、小于10s |
实验室制取的气体不能用浓硫酸干燥的是( )
| A、NH3 |
| B、C02 |
| C、02 |
| D、H2 |
有关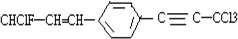 分子结构的叙述中,正确的是( )
分子结构的叙述中,正确的是( )
 分子结构的叙述中,正确的是( )
分子结构的叙述中,正确的是( )| A、除苯环以外的其余碳原子有可能都在一条直线上 |
| B、除苯环以外的其余碳原子在一条直线上 |
| C、12个碳原子不可能都在同一平面上 |
| D、12个碳原子有可能都在同一平面上 |
