题目内容
【题目】(1)①常温下,.某溶液中由水电离出的c(OH-)=1.0×10-10mol/L,该溶液可以是_________。(填选项)
A. pH=4的CH3COOH B.pH=10的NaOH C. pH=9的 Na2CO3
D. pH=2的 H2SO4 E. pH=4的 NH4C1
(2)常温下,aml/0.lmol/L盐酸与bmL0.lmol/L氨水混合,充分反应,若混合后溶液呈中性,则a____b (填“<”、“>”或“=”)。
(3)常温下,amLpH=3的盐酸与bmLpH=11的氨水混合,充分反应,若a=b,,则反应后溶液中离子浓度从大到小的顺序是___________。
(4)氯化铝水溶液呈酸性,原因是(用离子方程式表示〉:___________。把A1Cl3溶液蒸干,灼烧,最后得到的主要固体产物是___________。
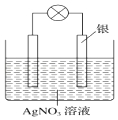
(5)25℃,在0.10 mol/LH2S溶液中,通入HC1气体或加入NaOH固体以调节溶液pH,溶液pH与c(S2-)关系如下图(忽略溶液体积的变化、H2S的挥发)。
① pH=13时,溶液中的 c(H2S)+c(HS-)=_________mol/L。
② 某溶液含 0.020 mol /LMn2+、0.10 mol/LH2S,当溶液pH=_____时,Mn2+开始沉淀。(Ksp(MnS) =2.8×1013)

【答案】 AB < c(NH4+)>c(Cl-)>c(OH-)>c(H+) Al3++3H2O![]() Al(OH)3+3H+ Al2O3 0.043 5
Al(OH)3+3H+ Al2O3 0.043 5
【解析】(1)A、pH=4的CH3COOH溶液中,c(H+)=10﹣4mol/L,根据水的离子积常数,可知c(OH﹣)= ![]() ,而溶液中OH﹣完全来自于水的电离,所以,水电离出的c(OH﹣)==1.0×10﹣10mol/L,故A正确;B、pH=10的NaOH溶液中,c(H+)=10﹣10mol/L,碱溶液中H+完全来自于水的电离,又因为水电离出H+与OH﹣相等,故水电离出的c(OH﹣)=c(H+)=1.0×10﹣10mol/L,故B正确;C、pH=9的Na2CO3溶液中,水解后,c(H+)=10﹣9mol/L,根据水的离子积可知c(OH﹣)=
,而溶液中OH﹣完全来自于水的电离,所以,水电离出的c(OH﹣)==1.0×10﹣10mol/L,故A正确;B、pH=10的NaOH溶液中,c(H+)=10﹣10mol/L,碱溶液中H+完全来自于水的电离,又因为水电离出H+与OH﹣相等,故水电离出的c(OH﹣)=c(H+)=1.0×10﹣10mol/L,故B正确;C、pH=9的Na2CO3溶液中,水解后,c(H+)=10﹣9mol/L,根据水的离子积可知c(OH﹣)= ![]() ,又Na2CO3的OH﹣全部来自于水的电离,故水电离出的c(OH﹣)= 1.0×10﹣5mol/L,故C错误;D、pH=2的硫酸溶液中,c(H+)=10﹣2mol/L,对水的电离起到抑制作用,酸溶液中氢氧根离子完全由水电离,水电离出的c(OH﹣)=
,又Na2CO3的OH﹣全部来自于水的电离,故水电离出的c(OH﹣)= 1.0×10﹣5mol/L,故C错误;D、pH=2的硫酸溶液中,c(H+)=10﹣2mol/L,对水的电离起到抑制作用,酸溶液中氢氧根离子完全由水电离,水电离出的c(OH﹣)= ![]() ,故D错误;E、NH4Cl属于强酸弱碱盐,促进水电离,pH=4的NH4Cl溶液中,c(H+)=10﹣4mol/L,水电离出的c(OH﹣)=c(H+)=10﹣4mol/L,故E错误;
,故D错误;E、NH4Cl属于强酸弱碱盐,促进水电离,pH=4的NH4Cl溶液中,c(H+)=10﹣4mol/L,水电离出的c(OH﹣)=c(H+)=10﹣4mol/L,故E错误;
故答案为:AB;
(2)a ml/0.lmol/L盐酸与b mL0.lmol/L氨水混合,假设a=b,则恰好完全反应生成氯化铵,溶液显酸性;若要显中性,则氨水应该过量。故答案为:<;
(3)pH=3的盐酸c(H+)= 10-3mol/L,而pH=11的氨水中,c(NH3·H2O)>c(OH-)=10-3mol/L,若a=b,反应后还有大量的NH3·H2O又电离出氢氧根离子,溶液呈碱性,溶液中电荷守恒分析,离子浓度的关系为:c(NH4+)>c(Cl﹣)>c(OH﹣)>c(H+);
故答案为:c(NH4+)>c(Cl﹣)>c(OH﹣)>c(H+);
(4)AlCl3为强酸弱碱盐,Al3+水解,溶液呈酸性,水解是微弱可逆的,故答案为:Al3++3H2O Al(OH)3+3H+;
(5)AlCl3水解化学方程式为:AlCl3+3H2O Al(OH)3+3HCl,其中HCl为易挥发性的酸,加热蒸干的过程中,HCl挥发,水解平衡不断向右移,蒸干之后得到Al(OH)3固体,灼烧Al(OH)3,分解得到Al2O3。故答案为:Al2O3;
(6) ①由图可知,pH=13时,c(S2﹣)=5.7×10﹣2mol/L,在0.10molL﹣1H2S溶液中根据硫守恒c(H2S)+c(HS﹣)+c(S2﹣)=0.10molL﹣1,所以c(H2S)+c(HS﹣)=0.1﹣5.7×10﹣2=0.043mol/L。
故答案为:0.043;
②当Qc=Ksp(MnS)时开始沉淀,Ksp(MnS)= c(Mn2+)·c(S2﹣),所以Mn2+开始沉淀时,c(S2﹣)= 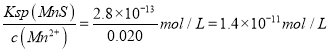 ,结合图象得出此时的pH=5。故答案为:5。
,结合图象得出此时的pH=5。故答案为:5。

【题目】表是元素周期表的一部分,请回答有关问题:
主族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | O |
2 | ① | ② | ③ | |||||
3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
(1)表中化学性质最不活泼的元素,其原子结构示意图为 .
(2)元素③、⑦、⑧中,原子半径从大到小的顺序是(用元素符号表示).
(3)元素④和⑥的最高价氧化物的水化物在水溶液中反应的离子方程式为 .
(4)元素⑤与元素⑧形成的化合物的电子式为 .
(5)①、②、⑦、⑧四种元素的最高价氧化物的水化物中酸性最强的是 . (填酸的化学式).
(6)⑤⑥两元素相比较,金属性较强的是(填名称),可以验证该结论的实验是(填字母). A.将在空气中放置已久的这两种元素的块状单质分别放入热水中
B.将形状、大小相同的这两种元素的单质分别和同浓度的盐酸反应
C.将形状、大小相同这两种元素的单质分别和热水作用,并滴入酚酞溶液
D.比较这两种元素的气态氢化物的稳定性.
【题目】(12分)已知:I2+2S2O===S4O+2I-。相关物质的溶度积常数见下表:
物质 | Cu(OH)2 | Fe(OH)3 | CuCl | CuI |
Ksp | 2.2×10-20 | 2.6×10-39 | 1.7×10-7 | 1.3×10-12 |
(1)某酸性CuCl2溶液中含有少量的FeCl3,为得到纯净的CuCl2·2H2O晶体,加入 ,(填化学式)调至pH=4,使溶液中的Fe3+转化为Fe(OH)3沉淀,此时溶液中的c(Fe3+)= 。过滤后,将所得滤液低温蒸发、浓缩结晶,可得到CuCl2·2H2O晶体。
(2)在空气中直接加热CuCl2·2H2O晶体得不到纯的无水CuCl2,原因是 (用化学方程式表示)。由CuCl2·2H2O晶体得到纯的无水CuCl2的合理方法是 。
(3)某学习小组用“间接碘量法”测定含有CuCl2·2H2O晶体的试样(不含能与I-发生反应的氧化性杂质)的纯度,过程如下:取0.36 g试样溶于水,加入过量KI固体,充分反应,生成白色沉淀。用0.1000 mol/L Na2S2O3标准溶液滴定,到达滴定终点时,消耗Na2S2O3标准溶液20.00 mL。
①可选用 作滴定指示剂,滴定终点的现象是 。
②CuCl2溶液与KI反应的离子方程式为 。
③该试样中CuCl2·2H2O的质量百分数为 。