题目内容
【题目】已知![]() 、
、![]() 、
、![]() 、
、![]() 为原子序数依次增大的短周期元素,
为原子序数依次增大的短周期元素,![]() 为地壳中含量最高的过渡金属元素,
为地壳中含量最高的过渡金属元素,![]() 与
与![]() 同主族,
同主族,![]() 与
与![]() 同周期,且
同周期,且![]() 与
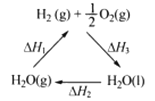
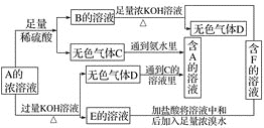
与![]() 的原子序数之和为20。甲、乙分别为元素E、A的单质, 丙、丁为A、E分别与B形成的二元化合物,它们转化关系如图所示。下列说法不正确的是( )
的原子序数之和为20。甲、乙分别为元素E、A的单质, 丙、丁为A、E分别与B形成的二元化合物,它们转化关系如图所示。下列说法不正确的是( )

A.![]() 、
、![]() 形成的一种化合物具有漂白性
形成的一种化合物具有漂白性
B.![]() 、
、![]() 形成的离子化合物可能含有非极性键
形成的离子化合物可能含有非极性键
C.![]() 的单质能与丙反应置换出
的单质能与丙反应置换出![]() 的单质
的单质
D.丁为黑色固体,且1mol甲与足量丙反应转移电子3 NA
【答案】D
【解析】
已知A、B、C、D为原子序数依次增大的短周期元素,E为地壳中含量最高的过渡金属元素,则E为Fe;![]() 与
与![]() 同主族,
同主族,![]() 与
与![]() 同周期,可知A、B、C、D分属三个不同的短周期,则A为H,D为Na,由
同周期,可知A、B、C、D分属三个不同的短周期,则A为H,D为Na,由![]() 与
与![]() 的原子序数之和为20,可知C为F;甲、乙分别为元素E、A的单质, 丙、丁为A、E分别与B形成的二元化合物,结合图示转化关系,由Fe与水蒸气反应生成四氧化三铁可知可知丙为H2O,丁为Fe3O4,则B为O元素,以此解答该题。
的原子序数之和为20,可知C为F;甲、乙分别为元素E、A的单质, 丙、丁为A、E分别与B形成的二元化合物,结合图示转化关系,由Fe与水蒸气反应生成四氧化三铁可知可知丙为H2O,丁为Fe3O4,则B为O元素,以此解答该题。
由以上分析可知:A为H,B为O,C为F,D为Na,E为Fe元素;甲为Fe,乙为H2,丙为H2O,丁为Fe3O4;
A.H、O两元素组成的H2O2有强氧化性,具有漂白性,故A正确;
B.O和Na组成的Na2O2中含有离子键和非极性共价键,故B正确;
C.F2溶于水生成HF和O2,故C正确;
D.丁为Fe3O4,是黑色固体,由3Fe+4H2O![]() Fe3O4+4H2可知1molFe与足量H2O反应转移电子
Fe3O4+4H2可知1molFe与足量H2O反应转移电子![]() NA,故D错误;
NA,故D错误;
故答案为D。

 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案【题目】满足下列条件的有机物的种类数正确的是
选项 | 有机物 | 条件 | 种类数 |
A | C5H10O2 | 在酸性条件下会水解生成甲和乙,且甲、乙的相对分子质量相等 | 4 |
B | C6H12O2 | 能与 NaHCO3溶液反应 | 3 |
C | C5H12O | 含有2个甲基的醇 | 5 |
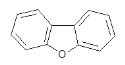
D |
| 该有机物的一氯代物 | 4 |
A.AB.BC.CD.D