题目内容
1.阅读下文,并回答(1)~(3)小题.20世纪90年代初,国际上提出了“预防污染”这一新概念.绿色化学是“预防污染”的根本手段,它的目标是研究和寻找能充分利用的无毒害原材料,最大限度地节约能源,在化工生产各五一节都实现净化和无污染的反应途径.
(1)下列各项属于“绿色化学”的是D
A.处理废弃物 B.治理污染点C.减少有毒物 D.杜绝污染源
(2)在国际环境问题中,一次性使用聚苯乙烯材料带来的“白色污染”极为严重.最近研制出一种新材料聚乳酸:
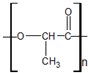
它能代替聚苯乙烯,它由乳酸聚合而成,能在乳酸菌的作用下,降解而消除对环境的污染.下列关于聚乳酸的说法正确的是B
A.聚乳酸的单体是
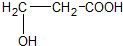
B.聚乳酸的单体自身分子间在一定条件下能够相互反应生成环状化合物
C.聚乳酸是一种羧酸
D.单体聚合成聚乳酸的方式与单体聚合成聚苯乙烯的方式相同
(3)1996年美国罗姆斯公司的G.L.Willingham等人研制出对环境安全的船舶防垢剂──“海洋9号”而获得了美国“总统绿色化学挑战奖”.“海洋9号”的结构简式如下式:
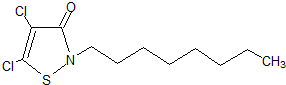
试回答下列问题:
①“海洋9号”的化学式为C11H17NSOCl2;
②“海洋9号”能在一定条件下与H2发生加成反应,写出“海洋9号”与足量氢气加成产物的结构简式
 ;
;③若“海洋9号”分子中的氢原子被一个氯原子取代,所得一氯取代物的种数为8.
分析 (1)根据绿色化学的含义判断,绿色化学是指环境友好化学,即无污染,其核心是从源头上消除污染;
(2)聚乳酸的单体为乳酸,由题中高分子可推得乳酸为 .乳酸聚合成聚乳酸得反应为缩聚反应,而单体聚合成聚苯乙烯的反应为加聚反应.因乳酸分子中既含有羟基又含有羧基,所以两分子乳酸可形成环状化合物:
.乳酸聚合成聚乳酸得反应为缩聚反应,而单体聚合成聚苯乙烯的反应为加聚反应.因乳酸分子中既含有羟基又含有羧基,所以两分子乳酸可形成环状化合物: ;
;
(3)①根据结构简式确定分子式;
②碳碳双键能与氢气加成;
③氢原子有8种.
解答 解:(1)A.处理废弃物是污染治理措施,污染已经产生,不是从源头消除污染,不符合绿色化学理念,故A错误;
B.治理污染点,污染已经产生,也不是从源头消除污染,不符合绿色化学理念,故B错误;
C.减少有毒物并没有根除有毒物质,也不是从源头消除污染,不符合绿色化学理念,故C错误;
D.杜绝污染源是从源头消除污染,符合绿色化学理念,故D正确;
故答案为:D;
(2)A.聚乳酸的单体为乳酸,由题中高分子可推得乳酸为 ,故A错误;
,故A错误;
B.乳酸分子中既含有羟基又含有羧基,所以两分子乳酸可形成环状化合物: ,故B正确;
,故B正确;
C.聚乳酸含有羟基,不是羧酸,故C错误;
D.乳酸聚合成聚乳酸得反应为缩聚反应,而单体聚合成聚苯乙烯的反应为加聚反应,故D错误.
故答案为:B;
(3)①根据 可知分子式为C11H17NSOCl2,故答案为:C11H17NSOCl2;
可知分子式为C11H17NSOCl2,故答案为:C11H17NSOCl2;
②“海洋9号”与足量氢气加成产物的结构简式 ,
,
故答案为: ;
;
③分子中每个碳原子均不对称,氢原子有8种,一氯取代物有8种,故答案为:8.
点评 本题涉及污染物处理、新物质的合成等,题目难度不大,在研究化学物质和化学反应时,要关心环境问题,要考虑“省资源、能源、少污染、减成本”的绿色化学的要求.

练习册系列答案
相关题目
15.下列化合物分子中,在核磁共振氢谱图中仅有一个吸收峰的是( )
| A. |  | B. | 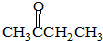 | C. | CH3OCH3 | D. | CH3CH2CH3 |
16.根据下列反应,判断氧化剂的氧化性强弱顺序为( )
①H2S+Cl2═S+2HCl
②2NaI+Cl2═2NaCl+I2
③Na2S+I2═2NaI+S.
①H2S+Cl2═S+2HCl
②2NaI+Cl2═2NaCl+I2
③Na2S+I2═2NaI+S.
| A. | Cl2>I2>S | B. | Cl2>S>I2 | C. | I2>Cl2>S | D. | S>I2>Cl2 |
13.下列物质都能与Na反应放出H2,其产生H2的速率排列顺序正确的是( )
①C2H5OH
②CH3COOH溶液
③H2O.
①C2H5OH
②CH3COOH溶液
③H2O.
| A. | ①>②>③ | B. | ②>①>③ | C. | ③>①>② | D. | ②>③>① |
10.可逆反应:3A(g)?3B(?)+C(?)△H>0,随着温度升高,气体平均相对分子质量有变小趋势,则下列判断正确的是( )
| A. | B和C可能都是固体 | B. | 若C为固体,则B一定是气体 | ||
| C. | B和C一定都是气体 | D. | B和C不可能都是气体 |
11.下列关于反应热的说法正确的是( )
| A. | 可逆反应“CO(g)+H2O(g)═CO2(g)+H2(g)”中的△H小于0,说明此反应为吸热反应 | |
| B. | 已知S(s)+O2(g)═SO3(g)的反应热为△H═-385.5kJ•mol-1,说明硫的燃烧热为385.5 kJ•mol-1 | |
| C. | 一个化学反应的反应热等于反应物的总能量减去生成物的总能量 | |
| D. | 化学反应的反应热只与反应体系的始态和终态有关,而与反应的途径无关 |
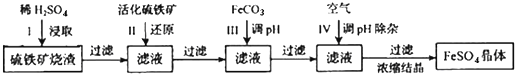
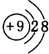 ,它是F-离子.1mo1B单质能从盐酸中置换出3g氢气,此时B转变为与Ne原子具有相同电子层结构的离子,则B元素是Al;B的最高价氧化物的对应水化物的化学式为Al(OH)3.C元素有3个电子层,且最外电子层比L电子层少2个电子,则C元素是SC与Na反应后生成物的电子式为
,它是F-离子.1mo1B单质能从盐酸中置换出3g氢气,此时B转变为与Ne原子具有相同电子层结构的离子,则B元素是Al;B的最高价氧化物的对应水化物的化学式为Al(OH)3.C元素有3个电子层,且最外电子层比L电子层少2个电子,则C元素是SC与Na反应后生成物的电子式为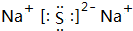 ,化合物中的化学键属于离子键.
,化合物中的化学键属于离子键.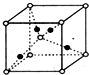 已知A、B、C、D、E、F均为前四周期元素.A元素的原子价电子排布为ns2np2,B元素的最外层电子数是其电子层数的3倍,C元素原子核外的M层中只有2对成对电子.D元素原子的M电子层的P能级中有3个未成对电子.B离子与E离子具有相同的电子层结构,可形成E2B2、E2B型化合物.F元素位于元素周期表的ds区,其原子与E原子具有相同的最外层电子数.
已知A、B、C、D、E、F均为前四周期元素.A元素的原子价电子排布为ns2np2,B元素的最外层电子数是其电子层数的3倍,C元素原子核外的M层中只有2对成对电子.D元素原子的M电子层的P能级中有3个未成对电子.B离子与E离子具有相同的电子层结构,可形成E2B2、E2B型化合物.F元素位于元素周期表的ds区,其原子与E原子具有相同的最外层电子数.