题目内容
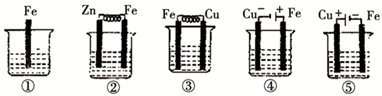
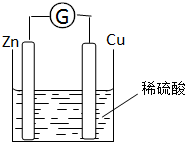
将锌片和铜片用导线相连浸入稀硫酸中组成原电池,两电极间连接一个电流计,装置如图:
(1)锌片上发生的电极反应:______;铜片上发生的电极反应:______;
(2)若该电池中两电极的总质量为60g,工作一段时间后,取出锌片和铜片洗净干燥后称重,总质量为47g,试计算产生标准状况氢气的体积为多少L?(请写出计算过程)______.
(1)锌片上发生的电极反应:______;铜片上发生的电极反应:______;
(2)若该电池中两电极的总质量为60g,工作一段时间后,取出锌片和铜片洗净干燥后称重,总质量为47g,试计算产生标准状况氢气的体积为多少L?(请写出计算过程)______.

1)该原电池中,锌易失电子发生氧化反应而作负极,电极反应式为:Zn-2e-=Zn2+,铜作正极,正极上氢离子得电子发生还原反应,电极反应式为:2H++2e-=H2↑,
故答案为:Zn-2e-=Zn2+;2H++2e-=H2↑;
(2)负极上锌生成锌离子进入溶液而导致质量减少,正极上氢离子得电子生成氢气,所以正极质量不变,两个电极减少的质量是锌的质量,锌和稀硫酸反应离子方程式为2H++Zn=Zn2++H2↑,
根据锌和氢气之间的关系式得氢气的体积=
×1×22.4L/mol=4.48L,
故答案为:4.48L.
故答案为:Zn-2e-=Zn2+;2H++2e-=H2↑;
(2)负极上锌生成锌离子进入溶液而导致质量减少,正极上氢离子得电子生成氢气,所以正极质量不变,两个电极减少的质量是锌的质量,锌和稀硫酸反应离子方程式为2H++Zn=Zn2++H2↑,
根据锌和氢气之间的关系式得氢气的体积=
| ||
| 1 |
故答案为:4.48L.

练习册系列答案
相关题目