题目内容
【题目】β紫罗兰酮是存在于玫瑰花、番茄等中的一种天然香料,它经多步反应可合成维生素A1。下列说法正确的是
 →……→
→……→ →……→
→……→
A.β紫罗兰酮与等物质的量的Br2加成反应可生成2种产物
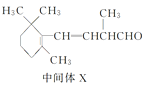
B.1 mol中间体X最多能与2 mol H2发生加成反应
C.维生素A1难溶于NaOH溶液
D.β紫罗兰酮与中间体X互为同分异构体
【答案】C
【解析】
A.β紫罗兰酮中存在共轭双烯,与等物质的量的Br2加成反应可以生成两种1,2-加成产物,一种1,4-加成产物,A项错误;
B.中间体X中还有碳碳双键、羰基,均可以与氢气发生加成,最多能与3 mol H2发生加成反应,B项错误;
C.维生素A1是多碳原子的烯醇,与氢氧化钠不反应,难溶于NaOH溶液,C项正确;
D.β紫罗兰酮与中间体X分子式不同,相差了一个CH2,结构相似,应互为同系物,不是同分异构体,D项错误;
答案选C。

练习册系列答案
相关题目