题目内容
【题目】研究NOx之间的转化具有重要意义。
(1)已知:N2O4(g) ![]() 2NO2(g) ΔH>0 将一定量N2O4气体充入恒容的密闭容器中,控制反应温度为T1。
2NO2(g) ΔH>0 将一定量N2O4气体充入恒容的密闭容器中,控制反应温度为T1。
①下列可以作为反应达到平衡的判据是________。
A.气体的压强不变 B.v正(N2O4)=2v逆(NO2) C.K不变 D.容器内气体的密度不变 E.容器内颜色不变
②t1时刻反应达到平衡,混合气体平衡总压强为p,N2O4气体的平衡转化率为75%,则反应N2O4(g) ![]() 2NO2(g)的平衡常数Kp=________(对于气相反应,用某组分B的平衡压强p(B)代替物质的量浓度c(B)也可表示平衡常数,记作Kp,如p(B)=p·x(B),p为平衡总压强,x(B)为平衡系统中B的物质的量分数)。
2NO2(g)的平衡常数Kp=________(对于气相反应,用某组分B的平衡压强p(B)代替物质的量浓度c(B)也可表示平衡常数,记作Kp,如p(B)=p·x(B),p为平衡总压强,x(B)为平衡系统中B的物质的量分数)。
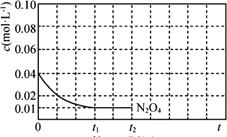
③反应温度T1时,c(N2O4)随t(时间)变化曲线如图,画出0~t2时段,c(NO2)随t变化曲线。保持其它条件不变,改变反应温度为T2(T2>T1),再次画出0~t2时段,c(NO2)随t变化趋势的曲线________。
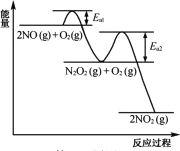
(2) NO氧化反应:2NO(g)+O2(g)=2NO2(g)分两步进行,其反应过程能量变化示意图如图。
Ⅰ 2NO(g)=N2O2(g) ΔH1
Ⅱ N2O2(g)+O2(g)→2NO2(g) ΔH2
①决定NO氧化反应速率的步骤是________(填“Ⅰ”或“Ⅱ”)。
②在恒容的密闭容器中充入一定量的NO和O2气体,保持其它条件不变,控制反应温度分别为T3和T4(T4>T3),测得c(NO)随t(时间)的变化曲线如图。转化相同量的NO,在温度_____(填“T3”或“T4”)下消耗的时间较长,试结合反应过程能量图分析其原因____。

【答案】AE ![]() p
p 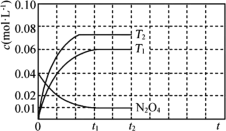 Ⅱ T4 ΔH1<0,温度升高,反应Ⅰ平衡逆移,c(N2O2)减小,浓度降低的影响大于温度对反应Ⅱ速率的影响
Ⅱ T4 ΔH1<0,温度升高,反应Ⅰ平衡逆移,c(N2O2)减小,浓度降低的影响大于温度对反应Ⅱ速率的影响
【解析】
(1)①化学反应平衡的判断可从以下几方面考虑:体系中所有反应物和生成物的质量(或浓度)保持不变,正反应速率等于逆反应速率;
②建立三段式求解可得;
③由图确定t1时反应生成的NO2浓度;该反应为吸热反应,升高温度,平衡向正反应方向移动;
(2)①由图可知,反应Ⅰ的活化能小于反应Ⅱ的活化能,活化能越大,反应速率越慢;
②由图可知,转化相同量的NO,在温度T4下消耗的时间较长,原因是浓度降低的影响大于温度对反应Ⅱ速率的影响。
(1)①A、该反应是一个气体体积减小的反应,气体的压强不变说明各物质浓度保持不变,反应达到化学平衡状态,故正确;
B、v正(N2O4)=2v逆(NO2)说明正逆反应速率不相等,反应没有达到化学平衡状态,故错误;
C、温度不变,化学平衡常数K不变,则K不变不能说明反应达到化学平衡状态,故错误;
D、由质量守恒定律可知,反应前后气体质量不变,恒容容器的体积不变,则密度始终不变,则密度不变不能说明反应达到化学平衡状态,故错误;
E、容器内颜色不变说明各物质浓度保持不变,反应达到化学平衡状态,故正确;
AE正确,故答案为:AE;
②设起始N2O4的物质的量为1mol,由题给数据建立如下三段式:
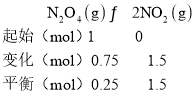
由三段式数据可知N2O4的平衡分压为![]() ×p=
×p=![]() ,NO2的平衡分压为
,NO2的平衡分压为![]() ×p=
×p=![]() ,则平衡常数Kp=
,则平衡常数Kp=![]() =
=![]() ,故答案为:
,故答案为:![]() ;
;
③由图可知,t1时反应消耗N2O4的浓度为(0.04—0.01)mol/L,由方程式可得反应生成NO2的浓度为0.03 mol/L×2=0.06 mol/L;该反应为吸热反应,升高温度,平衡向正反应方向移动,NO2的浓度增大,则0~t2时段,NO2的浓度c(NO2)随t变化趋势的曲线为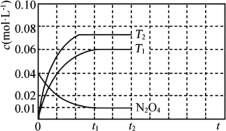 ,故答案为:
,故答案为: ;
;
(2)①由图可知,反应Ⅰ的活化能小于反应Ⅱ的活化能,活化能越大,反应速率越慢,则化学反应速率反应Ⅰ快于反应Ⅱ,化学反应取决于反应速率较慢的一步,则决定NO氧化反应速率的步骤是反应Ⅱ,故答案为:Ⅱ;
②由图可知,转化相同量的NO,在温度T4下消耗的时间较长,原因是反应Ⅰ为放热反应,温度升高,反应Ⅰ平衡逆移,c(N2O2)减小,浓度降低的影响大于温度对反应Ⅱ速率的影响,导致转化相同量的NO,在温度较高的T4下消耗的时间较长,故答案为:T4;反应Ⅰ为放热反应,温度升高,反应Ⅰ平衡逆移,c(N2O2)减小,浓度降低的影响大于温度对反应Ⅱ速率的影响;

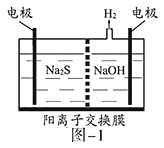
【题目】已知氯气和氢氧化钠的反应条件不同,产物也不同,在实验室里可用如图所示装置制取氯酸钠次氯酸钠和探究氯水的性质。
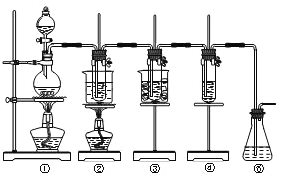
图中:①为氯气发生装置;②的试管里盛有15mL 30% NaOH溶液,并置于热水浴中;
③的试管里盛有15mL 8%NaOH溶液,并置于冰水浴中;④的试管里加有紫色石蕊试液;⑤为尾气吸收装置。请填写下列空白:
(1)制取氯气时,在烧瓶里加入一定量的二氧化锰,通过_________(填写仪器名称)向烧瓶中加入适量的浓盐酸。实验时为了除去氯气中的氯化氢气体,可在①与②之间安装盛有_________(填写下列编号字母)的净化装置。
A.碱石灰 | B.饱和食盐水 | C.浓硫酸 | D.饱和碳酸氢钠溶液 |
(2)比较制取氯酸钠和次氯酸钠的条件,指出二者的差异:______________________。
(3)本实验中制取次氯酸钠的离子方程式是__________________________________。
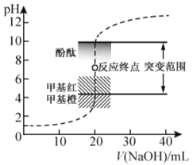
(4)实验中可观察到④的试管里溶液的颜色发生了如下变化,请填写下表中的空白:
实验现象 | 原因 |
溶液最初从紫色逐渐变为_______色 | 氯气与水反应生成的H+使石蕊变色 |
随后溶液逐渐变为无色 | _________________ |
然后溶液从无色逐渐变为_______色 | __________________________________ |
【题目】某同学通过实验研究Na2O2与水的反应。
操作 | 现象 |
向盛有少量Na2O2的试管中加入蒸馏水,得到溶液a | 反应剧烈,产生能使带火星木条复燃的气体 |
然后向溶液a中滴入两滴酚酞 | 溶液先变红,再逐渐变浅,约10分钟溶液变为无色 |
为了探究溶液变为无色的原因,该同学按照科学的程序,进行了如下实验:
(推理与假设)
Na2O2与H2O反应的化学方程式_____。向溶液a中滴加酚酞本应只会变红,而实验中发现酚酞变红后又褪色。由此提出如下的假设:
假设A:O2有漂白性 假设B:NaOH有漂白性 假设C:O2和NaOH共同作用有漂白性
(实验与观察)
(2)请完成下表:
实验编号 | 1 | 2 | 3 |
实验装置 |
|
|
|
实验假设 (填“A”、“B”或“C”) | 假设_____ | 假设____ | 假设__ |
实验现象 | 溶液变红后10分钟均无变化 | ||
实验结论 | _____ | ||
(查阅资料)
该同学查阅资料:H2O2是一种在碱性条件下不稳定、具有漂白性的物质。
(推理与假设)
该同学认为褪色的原因可能是溶液a中存在H2O2,H2O2漂白了酚酞。
(实验与观察)
(3)通过实验证实了H2O2的存在:取少量溶液a,加入黑色粉末____(填化学式),快速产生了能使带火星木条复燃的气体。该同学进一步通过实验证实了溶液a中滴入酚酞后,H2O2与酚酞发生了化学反应。实验方案:取少量溶液a于试管中,_____。
(解释与结论)
(4
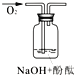
【题目】以SO2、软锰矿(主要成分为MnO2,少量Fe、Al、Ca及Pb的化合物等)、氨水及净化剂等为原料可制备MnSO4液和Mn3O4,主要实验步骤如下
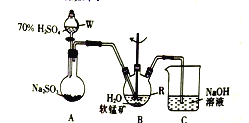
步骤I、如图所示装置,将SO2通入B中的软锰矿浆液中(MnO2+SO2=MnSO4)。
步骤II、充分反应后,在不断搅拌下依次向仪器R中加入适量纯净的MnO2、MnCO3,最后加入适量Na2S沉铅,
步骤III、过滤得MnSO4溶液
(1)仪器R的名称是_______。
(2)装置A用于制取SO2,反应的化学方程式为_________。
(3)装置B中的反应应控制在90~100℃,适宜的加热方式是______________。
(4)装置C的作用是______________________。
(5)“步骤Ⅱ”中加入纯净MnO2的目的是_______________,用MnCO3调节溶液pH时,需调节溶液pH的范围为________(该实验条件下,部分金属离子开始沉淀和沉淀完全的pH如下表)
金属离子 | Fe2+ | Fe3+ | Al3+ | Mn2+ |
开始沉淀的pH | 7.04 | 1.87 | 3.32 | 7.56 |
沉淀完全的pH | 9.18 | 3.27 | 4.9 | 10.2 |
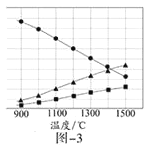
(6)已知①用空气氧化Mn(OH)2浊液可制备Mn3O4[6Mn(OH)2+O2![]() 2Mn3O4+6H2O],主要副产物为MnOOH;反应温度和溶液pH对产品中Mn的质量分数的影响分别如图所示
2Mn3O4+6H2O],主要副产物为MnOOH;反应温度和溶液pH对产品中Mn的质量分数的影响分别如图所示

②反应温度超过80℃时,Mn3O4的产率开始降低,Mn(OH)2是白色沉淀,Mn3O4呈黑色;Mn3O4、MnOOH中锰的质量分数理论值依次为72.05%、62.5%请补充完整由步骤III得到MnSO4溶液,并用氨水等制备较纯净的Mn3O4的实验方案:______________________,真空干燥6小时得产品Mn3O4。