题目内容
【题目】下列说法不正确的是
A.常温下,在0.1mol·L-1的HNO3溶液中,由水电离出的c(H+)<![]()
B.浓度为0.1mol·L-1的NaHCO3溶液:c(H2CO3)>c(CO32-)
C.25℃时,AgCl固体在等物质的量浓度的NaCl、CaCl2溶液中的溶度积相同
D.冰醋酸中逐滴加水,溶液的导电性、醋酸的电离程度、pH均先增大后减小
【答案】D
【解析】
试题分析:A.硝酸是强酸抑制水的电离,则常温下,在0.1mol·L-1的HNO3溶液中,由水电离出的c(H+)=10—13mol/L<![]() ,A正确;B.浓度为0.1mol·L-1的NaHCO3溶液显碱性,碳酸氢根的水解程度大于电离程度,则c(H2CO3)>c(CO32-),B正确;C.溶度积常数只与温度有关系,则25℃时,AgCl固体在等物质的量浓度的NaCl、CaCl2溶液中的溶度积相同,C正确;D.稀释促进电离,则冰醋酸中逐滴加水,溶液的导电性先增大后减小,而醋酸的电离程度一直增大,pH先减小后增大,D错误,答案选D。
,A正确;B.浓度为0.1mol·L-1的NaHCO3溶液显碱性,碳酸氢根的水解程度大于电离程度,则c(H2CO3)>c(CO32-),B正确;C.溶度积常数只与温度有关系,则25℃时,AgCl固体在等物质的量浓度的NaCl、CaCl2溶液中的溶度积相同,C正确;D.稀释促进电离,则冰醋酸中逐滴加水,溶液的导电性先增大后减小,而醋酸的电离程度一直增大,pH先减小后增大,D错误,答案选D。

 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案【题目】某研究性学习小组设计实验用30mL浓硫酸与10mL无水乙醇共热制备乙烯气体、并测定乙醇转化成乙烯的转化率。已知生成的乙烯气体中含有SO2、CO2、乙醇和乙醚等杂质。有关数据如下:
熔点/℃ | 沸点/℃ | 溶解性 | 颜色状态 | 密度g/cm3 | |
乙醇 | -114.1 | 78.3 | 与水、有机溶剂互溶 | 无色液体 | 0.79 |
乙醚 | -116.2 | 34.5 | 不溶于水,易溶于有机溶剂 | 无色液体 | 0.7135 |
(1)制备乙烯
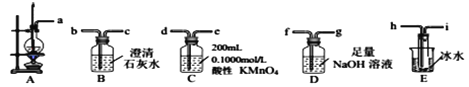
① 从A~E中选择必要的装置完成实验,并按气流方向连接的顺序为________(填仪器接口的字母编号)。
② D装置中发生反应的离子方程式______实验后,检验D溶液中含有CO32-的实验方案为_____。
③ E装置的主要作用是__________________。
(2)测定乙烯反应结束后,用移液管移取C中溶液20mL(不考虑溶液体积变化)于锥形瓶中,先加入约2mL稀硫酸酸化.再用0.1000mol/L的Na2C2O4溶液滴定未反应完的KMnO4。
已知:C2H4 ![]() CO2+H2O;C2O42-
CO2+H2O;C2O42- ![]() CO2+H2O;MnO4-→Mn2+
CO2+H2O;MnO4-→Mn2+
④ 以下情况使得测定乙烯的量偏高的是______
A.在用蒸馏水清洗碱式滴定管后,直接装Na2C2O4标准液
B.锥形瓶清洗干净后残有大量水珠
C.滴定前,滴定管内无气泡,滴定后有气泡
D.读数时,滴定前平视,滴定后俯视
⑤ 滴定终点的现象为_______________。
⑥ 已知用去Na2C2O4溶液20.00mL,则乙醇转化成乙烯的转化率为_________。(小数点后保留2位数字)
【题目】实验室欲配制1mol/L NaOH溶液240ml,请回答:
(1)需称取NaOH固体____________g,用质量为23.1 g的烧杯放在托盘天平上称取所需NaOH固体时,请在附表中选取所需的砝码大小___________(填字母),并在下图中选出能正确表示游码位置的选项____________(填字母)。
附表砝码规格
a | b | c | d | e | |
砝码大小/g | 100 | 50 | 20 | 10 | 5 |

(2)选用的主要玻璃仪器除烧杯、玻璃棒外还有_____________________________。
(3)下列操作的顺序是(用序号表示)_________________。
A、用30mL水洗涤烧杯2—3次,洗涤液均注入容量瓶,振荡
B、用天平准确称取所需的NaOH的质量,加入少量水,用玻璃棒慢慢搅动,使其充分溶解
C、将已冷却的NaOH溶液沿玻璃棒注入容量瓶中
D、将容量瓶盖紧,颠倒摇匀
E、改用胶头滴管加水,使溶液凹面恰好与刻度相切
F、继续往容量瓶内小心加水,直到液面接近刻度1—2cm处
(4)下列情况对所配制的NaOH溶液浓度有何影响?(用“偏大”“偏小”“无影响”填写)
①容量瓶用蒸馏洗涤后残留有少量的水________________
②将热的溶液直接移入了容量瓶________________
③定容时,仰视容量瓶的刻度线________________
④转移溶液时,玻璃棒的下端在容量瓶的刻度线以上________________