题目内容
1.9.03×1023个CH4中,含1.5mol碳原子,6mol氢原子,15mol电子.标准状况下,CH4所占的体积为33.6 L.分析 结合n=$\frac{N}{{N}_{A}}$及分子构成计算.
解答 解:9.03×1023个CH4的物质的量为$\frac{9.03×1{0}^{23}}{6.02×1{0}^{23}}$=1.5mol,则含C为1.5mol,含H为1.5mol×4=6mol,电子1.5mol×10=15mol,标准状况下,CH4所占的体积为1.5mol×22.4L/mol=33.6L,故答案为:1.5; 6;15;33.6L.
点评 本题考查物质的量的计算,为高频考点,把握微粒数、物质的量的关系为解答的关键,侧重分析与计算能力的考查,注意基本计算公式的应用,题目难度不大.

练习册系列答案
 导学全程练创优训练系列答案
导学全程练创优训练系列答案
相关题目
11.如图所示的实验操作中,正确的是( )
| A. |  | B. | 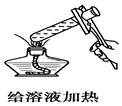 | C. | 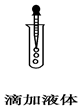 | D. | 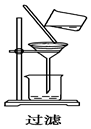 |
9.常温下,下列有关溶液的说法不正确的是( )
| A. | Na2CO3、NaHCO3两种盐溶液中,离子种类相同 | |
| B. | 物质的量浓度相同的NH4Cl和NH4HSO4两种溶液中,c(NH4+)前者小于后者 | |
| C. | 某物质的水溶液中由水电离出的c(H+)=1×10-amol/L,若a>7,则该溶液的pH为a或14-a | |
| D. | 相同温度下,0.2mol/L的醋酸溶液与0.1mol/L的醋酸溶液中c(H+)之比大于2:1 |
6.下列说法正确的是( )
| A. | 摩尔是用来衡量微观粒子多少的一种物理量 | |
| B. | 标况下O2的体积取决于O2分子间的距离 | |
| C. | 常温常压下4.9LO3含有的O约为9.6g | |
| D. | 若气体摩尔体积为22.4 L/mol,则所处条件为标准状况 |
13.下列分子中,属于含有极性键的非极性分子的一组是( )
| A. | SO2、CCl4 | B. | BF3、CO2 | C. | H2、N2 | D. | NH3、H2O |
10.下列实验装置或操作不符合实验要求的是( )
| A. | 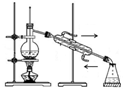 石油分馏 | B. |  灼烧干海带 | C. |  分离汽油和水 | D. |  冶炼金属铁 |
2.美国探测发现,在土卫六上的碳氢化合物储量是地球上的几百倍.对此,有关说法不正确的是( )
| A. | 碳氢化合物就是我们所说的烃 | |
| B. | 这一发现可以为我们提供足够的化石燃料,从而减少开发新能源的投资 | |
| C. | 从石油中可以获得重要的有机化工原料--乙烯 | |
| D. | 相同质量的碳氢化合物中氢的质量分数越高,完全燃烧时消耗的O2越多 |