题目内容
10.下列实验装置或操作不符合实验要求的是( )| A. | 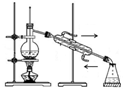 石油分馏 | B. |  灼烧干海带 | C. |  分离汽油和水 | D. |  冶炼金属铁 |
分析 A.分馏需要酒精灯、蒸馏烧瓶、冷凝管等,温度计测定馏分的温度;
B.灼烧在坩埚中进行;
C.汽油与水分层;
D.点燃Mg条,引发铝热反应可冶炼Fe.
解答 解:A.分馏需要酒精灯、蒸馏烧瓶、冷凝管等,温度计测定馏分的温度,则图中温度计的水银球应在支管口处,故A错误;
B.灼烧在坩埚中进行,图中装置可灼烧干海带,故B正确;
C.汽油与水分层,可利用图中装置分液,故C正确;
D.点燃Mg条,引发铝热反应可冶炼Fe,图中装置可冶炼金属Fe,故D正确;
故选A.
点评 本题考查化学实验方案的评价,为高频考点,把握混合物分离提纯实验、金属冶炼、实验装置的作用为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.

练习册系列答案
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案
相关题目
20.下列叙述正确的是( )
| A. | 通常情况下,1.5molO2的体积约为33.6L | |
| B. | NaOH的摩尔质量是40g | |
| C. | 100 mL水中溶解5.85gNaCl所得NaCl溶液的物质的量浓度为1 mol•L-1 | |
| D. | 任何条件下,等物质的量的水和一氧化碳所含有的分子数必相等 |
5.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 常温常压下,60g甲醛、乙酸与葡萄糖混合物充分燃烧消耗氧气分子数为3NA | |
| B. | 用惰性电极电解CuSO4溶液后,如果加入0.1 mol Cu(OH)2能使溶液复原,则电路中转移电子的数目为0.2NA | |
| C. | 已知3BrF3+5H2O=HBrO3+Br2+9HF+O2↑ 如果有5 mol H2O参加氧化还原反应,则由水还原的BrF3分子数目为3NA | |
| D. | 142 g Na2SO4和Na2HPO4固体混合物中,阴阳离子总数为3NA |
2.下列说法正确的是( )
| A. | CO2气体不能支持任何物质的燃烧 | |
| B. | 铝合金的硬度、熔点比组成合金各成分金属的大 | |
| C. | 将一小块钠放入足量AlCl3溶液中,最终有沉淀生成的 | |
| D. | 常温下,金属镁、铝在空气中都能与氧气反应,所以它们在空气中不能稳定存在 |
10.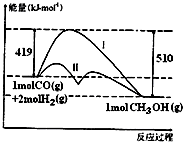 对于反应CO(g)+2H2(g)?CH3OH(g)△H,反应过程中的能量变化情况如图所示,曲线I和曲线II分别表示不使用催化剂和使用催化剂的两种情况.下列判断正确的是( )
对于反应CO(g)+2H2(g)?CH3OH(g)△H,反应过程中的能量变化情况如图所示,曲线I和曲线II分别表示不使用催化剂和使用催化剂的两种情况.下列判断正确的是( )
 对于反应CO(g)+2H2(g)?CH3OH(g)△H,反应过程中的能量变化情况如图所示,曲线I和曲线II分别表示不使用催化剂和使用催化剂的两种情况.下列判断正确的是( )
对于反应CO(g)+2H2(g)?CH3OH(g)△H,反应过程中的能量变化情况如图所示,曲线I和曲线II分别表示不使用催化剂和使用催化剂的两种情况.下列判断正确的是( )| A. | 该反应的△H=+91kJ/mol | |
| B. | 加入催化剂,该反应的△H变小 | |
| C. | 反应物的总能量大于生成物的总能量 | |
| D. | 如果该反应生成液态CH3OH时为△H1,则△H1>△H |
11.下列物质的水溶液因水解而呈酸性的是( )
| A. | HCl | B. | NH4Cl | C. | CH3COONa | D. | NaHCO3 |
 (1)写出电解饱和食盐水的离子方程式2Cl-+2H2O$\frac{\underline{\;通电\;}}{\;}$2OH-+H2↑+Cl2↑
(1)写出电解饱和食盐水的离子方程式2Cl-+2H2O$\frac{\underline{\;通电\;}}{\;}$2OH-+H2↑+Cl2↑